東工大ニュース
東工大ニュース
公開日:2014.05.16
東京工業大学資源化学研究所の庄子良晃助教と福島孝典教授、東京大学大学院薬学系研究科の内山真伸教授らの研究グループは、芳香環のみが置換した「結合の手を2本しか持たないホウ素のカチオン化合物(ボリニウムイオン)」の合成に世界で初めて成功しました。この化合物は、ホウ素がオクテット則(用語1)から著しく逸脱した電子不足化学種であり、これまで合成が極めて困難であるとされていました。さらに、ボリニウムイオンを用いて、安化学的に安定な二酸化炭素から酸素を奪うという特異な反応性を示すことを実証しました。これはボリニウムイオンの極めて高いルイス酸性(用語2)により、二酸化炭素がユニークな活性化を受けたことを示すものです。今後、「超ルイス酸分子化学」という新しい研究が加速するものと期待さます。
この成果は、11日に英国の科学誌「ネイチャー・ケミストリー(Nature Chemistry)」の電子版に先行掲載されました。
ホウ素化合物の性質や反応性は、その電子不足性とホウ素の低い電気陰性度に特徴づけられる。最も典型的なホウ素化合物は、中性三配位構造のボランである(図1)。この状態では、ホウ素は結合の手を三本持っている。この時、ホウ素上には空の2p軌道が存在し、ここに電子対を受け取ることで安定化する。すなわち、中性三配位のホウ素化合物はルイス酸として振る舞う。このようなボランの反応性は、「オクテット則」により説明できる。オクテット則とは、化学種が「構成する典型元素の価電子の数が8個になるように反応する」という経験則であり、化学の基本原理である。
それでは、中性のボランからさらに結合の手を一本取り去った化合物はどのようなものであろうか?そして、その化合物はどのような反応性を示すだろうか?結合の手を2本しか持たないホウ素のカチオン化合物は「ボリニウムイオン」と呼ばれている(図1)。
研究グループは、これまで安定に存在し得ないとされてきた、芳香環のみが置換したボリニウムイオンの単離に世界で初めて成功し、その強いルイス酸性に基づく特異な反応性を明らかにした。
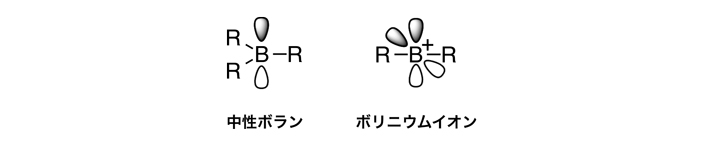
図1. 中性ボランとボリニウムイオンの構造。ホウ素原子の上下のローブは、空の2p軌道を表す。
同グループは、ボリニウムイオンのデザイン戦略として、①ホウ素上の置換基として適度な立体障害(用語3)をもつ芳香環であるメシチル基(2,4,6-トリメチルフェニル基)を用いること、および②対アニオンとして化学的に安定なアニオン種を用いることによって、芳香環のみが置換したボリニウムイオンの単離に初めて成功した。
ボリニウムイオンの詳細な分子構造は、各種分光分析に加え、単結晶X線構造解析により明らかにした(図2)。このボリニウムイオンは熱的に極めて安定であり、カルボラン塩の場合、結晶試料を300 ℃程度まで加熱しても分解しない。また、実験結果と理論化学計算の比較により、溶液、固体状態のいずれにおいても、ボリニウムイオンのホウ素中心は対アニオンや溶媒の配位を受けていないことが明らかとなった。さらに、理論化学計算の結果、ボリニウムイオンの最低非占有軌道(用語4)のエネルギー準位は、既存のホウ素化合物のものと比較して著しく低い -5.41 eV(電子ボルト)と算出された。以上の検討結果は、今回、合成したボリニウムイオンが熱力学的に安定でありつつも、同時に極めて高いルイス酸性を有していることを示している。
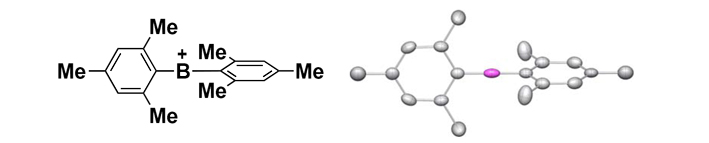
図2. ボリニウムイオンの結晶構造。
このボリニウムイオンの高い反応性を示す結果として、特異な二酸化炭素の活性化反応も見出した。ボリニウムイオンの溶液に二酸化炭素ガスを混合すると、二酸化炭素の炭素原子にボリニウムイオンのメシチル基が移り、かつ酸素を一つ失ったカチオン化合物が速やかに生成した(図3)。すなわちこの反応では、二酸化炭素の酸素原子がホウ素により奪われている。この特異な反応は、強いルイス酸中心であるボリニウムイオンのホウ素原子が、二酸化炭素の酸素原子に配位することから進行すると考えられる。実際、理論化学計算による考察では、この反応機構がエネルギー的に妥当であることが示された。本反応は、一般的に求核剤(用語5)を用いて行われる二酸化炭素の活性化反応とは全く異なる。ボリニウムイオンを利用することで、今後、様々な基質をターゲットとしたユニークな分子活性化が可能になると期待できる。
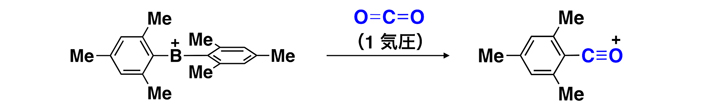
図3. ボリニウムイオンによる二酸化炭素の脱酸素化-アリール化反応。
同研究グループにより、芳香環のみが置換したボリニウムイオンの単離が可能であることが初めて実証された。また、ボリニウムイオンの特異な反応性も明らかになった。今後、ホウ素上の置換基として様々なアリール基やアルキル基を導入することで、「単離可能な究極のルイス酸分子」の創製を目指す。また、これらの研究を推進することで、新たな「超ルイス酸分子化学」の開拓に取り組む。
用語説明
(1) オクテット則 : 化学種を構成する元素の価電子数が8個になるように反応するという経験則であり、化学の基本原理。主に、第二周期の典型元素に適用される。
(2) ルイス酸 : ルイスによる酸の定義であり、電子対を受け取る物質を指す。それに対して、塩基は電子対を供与する物質と定義される。すなわち、ルイス酸は電子対受容体、ルイス塩基は電子対供与体である。
(3) 立体障害 : 立体的な嵩高さを指す。立体障害の大きい置換基が導入された部位は、他の分子と反応しにくくなる。
(4) 最低非占有軌道 : 電子によって占有されていない分子軌道のうち、最もエネルギーの低い軌道を指す。他の分子から電子対を受け取る反応などは、この最低非占有軌道が関わる。
(5) 求核剤 : 化学反応において電子密度が低い原子と反応する化学種を指す。二酸化炭素との反応であれば、求核剤は電子密度が最も低い炭素原子に対して反応し(求核攻撃)、結合を生成する。
論文情報
A two-coordinate boron cation featuring C-B+-C bonding
Yoshiaki Shoji, Naoki Tanaka, Koichiro Mikami, Masanobu Uchiyama & Takanori Fukushima,
Nature Chemistry (2014); doi:10.1038/nchem.1948
本論文は同誌のNews & Viewsにてハイライトされました。
Main-group chemistry: Boron served straight up
Christian Reus & Matthias Wagner,
Nature Chemistry (2014); doi:
10.1038/nchem.1953
お問い合わせ先
東京工業大学資源化学研究所・教授 福島 孝典
TEL: 045-924-5220
FAX: 045-924-5976
Email: fukushima@res.titech.ac.jp