東工大ニュース
東工大ニュース
公開日:2015.04.03
JST戦略的創造研究推進事業において、東京工業大学の細野 秀雄教授、原亨和教授、北野政明准教授らは、以前開発した常圧下で優れたアンモニア合成活性を持つルテニウム担持12CaO・7Al2O3エレクトライド[用語1])を触媒に用いると、強固な窒素分子の切断が容易になり、アンモニア合成で速度の最も遅い律速段階[用語2])が窒素分子の解離過程ではなく、窒素-水素結合形成過程となることを見いだしました。
アンモニアは、窒素肥料原料として膨大な量が生産されており、最近では燃料電池などのエネルギー源(水素エネルギーキャリア)としても期待が高まっています。これまでどの触媒[用語3]を用いても、強固な三重結合を持つ窒素分子の切断に高温、高圧の条件が必要であったため、アンモニア合成は多大なエネルギーを消費するプロセスとなっていました。
本研究グループは、同位体[用語4]を用いた窒素交換反応に計算科学を導入することで、この触媒上では窒素分子の切断の活性化エネルギー[用語5]が既存触媒の半分以下に低減し、その切断反応がアンモニア合成の律速段階ではないことを見いだしました。また、速度論解析[用語6]や水素吸蔵特性[用語7]を調べることで、エレクトライド触媒の水素吸蔵特性が反応メカニズムに大きな影響を与え、窒素-水素の結合の形成過程が律速段階であることを示唆しました。
今回の成果により、アンモニア合成プロセスの省エネルギー化に向けた触媒開発の有力な手がかりが得られたといえます。今後、この結果を利用したさまざまな化学反応への応用が期待できます。
本成果は、AccelプログラムにおいてPNNL(パシフィック・ノースウェスト・ナショナル・ラボラトリー、米国)のピーター・スシュコ博士らと共同で行ったものです。
本研究成果は、2015年3月30日(英国時間)に英国科学誌「Nature Communications」のオンライン速報版で公開されました。
本成果は、以下の事業・研究課題によって得られました。
戦略的創造研究推進事業 ACCEL
研究課題名 : |
|
代表研究者 : |
東京工業大学 元素戦略研究センター センター長 細野 秀雄 |
PM : |
科学技術振興機構 横山 壽治
|
研究実施場所 : |
東京工業大学
|
研究開発期間 : |
2013年10月~2018年3月
|
人工的にアンモニアを合成する技術は、ハーバーとボッシュによって初めて見いだされ、この技術(ハーバー・ボッシュ法、HB法)は、1912年代に工業的に完成してから約100年経った現在でも、人類の生活を支えるために必要不可欠となっています。また、アンモニア分子は分解することで多量の水素発生源となり、かつ室温・10気圧で液体になることから、燃料電池などのエネルギー源である水素運搬物質としても期待されています。
HB法の鍵は反応を速やかに進行させる触媒であり、鉄やルテニウムを含む多くの触媒が開発されてきました。アンモニア合成反応では、窒素分子の三重結合が極めて強固で安定なので、それを切断するのに大きなエネルギーを要してしまい、その結果として、どの触媒を用いても窒素分子の結合を切断する過程が全体の反応の速度を遅くしていること(律速)が知られていました。
本研究で用いた触媒は、C12A7エレクトライドという細野教授らが2003年に開発した物質の表面に、ナノサイズのルテニウムの微粒子を担持させたものであり、従来の触媒よりも効率よくアンモニアを合成できることを2012年に報告していました。しかし、その反応メカニズムの詳細は明らかになっていませんでした。
本研究では、当グループが開発したエレクトライドを担体に用いた触媒を使うと、これまでのアンモニア合成用触媒と比較して、以下のように反応メカニズムが大きく異なることが分かりました。
具体的には、窒素ガス(14N2、質量数28)と同位体窒素ガス(15N2、質量数30)が混ざったガス中で触媒を加熱すると、触媒表面上で窒素分子の切断反応と再結合反応が起こり、質量数29の窒素分子(14N15N)が生成します。この質量数29の窒素分子の生成速度をもとに、各触媒の窒素切断反応の速度を調べたところ、図1に示すようにC12A7エレクトライドにルテニウムを担持した触媒は、他のどのルテニウム触媒よりも低温での窒素切断反応に対する活性が高く、その活性化エネルギーは他の触媒の半分以下となりました。このことから、C12A7エレクトライドの強い電子供与能(電子を他に与える能力)によって、ルテニウム触媒の性能が大きく向上し、強固な窒素―窒素三重結合を効率よく切断できることが明らかとなりました。さらに、この速度論解析結果と量子化学計算を組み合わせることで、この触媒を用いたアンモニア合成反応の律速段階が窒素の切断過程ではないことが明らかとなりました。
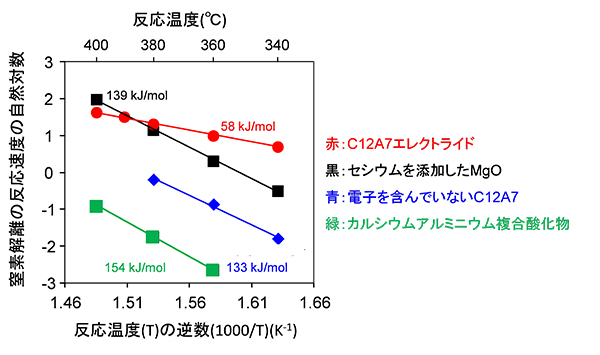
図1. さまざまな材料にルテニウムを担持した触媒を用いた窒素分子切断反応
C12A7エレクトライドにルテニウムを担持した触媒が、他の触媒の半分以下の活性化エネルギーを示すことが確認できます。
C12A7エレクトライドにルテニウムを担持した触媒は、300℃以上の反応温度において水素の吸蔵と放出挙動を示し、他の材料ではこのような挙動は見られませんでした(図2)。また、320℃よりも高い温度と低い温度で活性化エネルギーが変化することも明らかとなりました(図3)。つまり、320℃を境に反応メカニズムが変化していることが分かります。C12A7エレクトライドは水素中で加熱するとケージ内に水素をH-イオンとして吸蔵することが可能であり、さらに取り込んだH-イオンは水素として再び放出することもできます。これらの結果から、300℃以上の反応温度において窒素切断の促進効果に加えて水素吸蔵効果も反応メカニズムに多大な影響を及ぼしていることが分かりました。
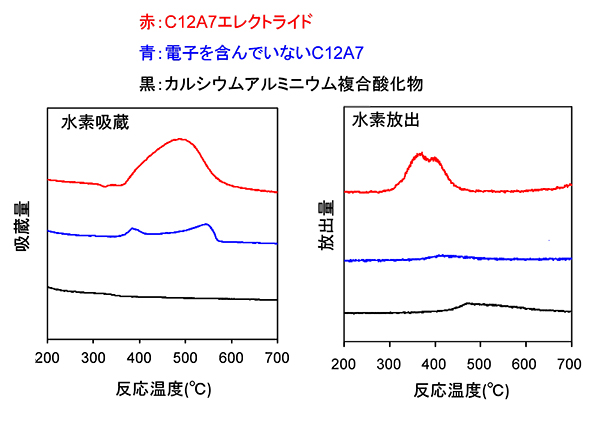
図2. さまざまな材料にルテニウムを担持した触媒の水素吸蔵と水素放出挙動
ルテニウムを担持したC12A7エレクトライドはアンモニア合成温度領域(300度以上)で水素の吸蔵と放出をすることが確認できます。
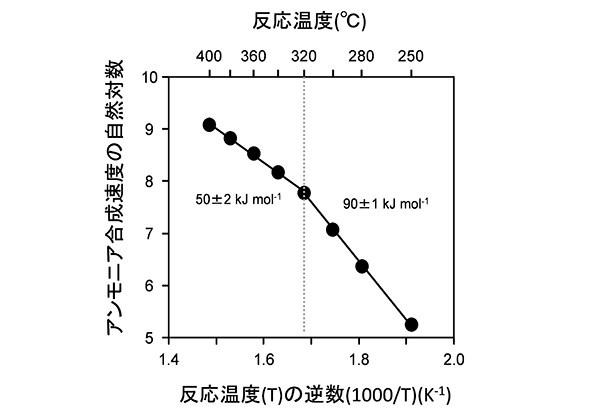
図3. さまざまな温度でルテニウムを担持したC12A7エレクトライドを用いてアンモニア合成反応を行った結果
320℃を境に活性化エネルギーが変化していることが確認できます。
以上の結果から既存の触媒との反応メカニズムの違いをまとめると(図4)、既存の触媒では、窒素分子の切断が律速段階であり、生成した窒素原子と水素原子が触媒表面上で反応しアンモニアが生成します。一方、C12A7エレクトライド触媒では、C12A7エレクトライドの電子がルテニウムのナノ粒子上に吸着した窒素分子に移動するために、窒素分子が原子に速やかに解離し、同時にルテニウム上で切断された水素が、C12A7エレクトライドのカゴの中にH-イオンとして収納されます。さらに、このH-イオンが原子状水素として放出され、窒素原子と反応することでアンモニアが生成されると考えられます。このようにアンモニア合成の律速段階が窒素分子の切断から窒素解離の次に障壁の高い窒素―水素結合の形成過程に変化することを明らかにしました。
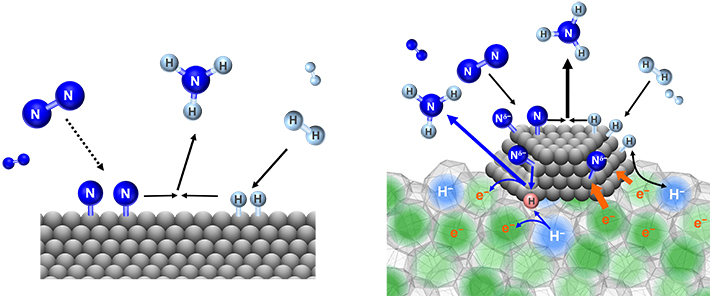
図4. 既存触媒とルテニウムを担持したC12A7エレクトライド上でのアンモニア合成のメカニズム
C12A7エレクトライドは、カゴの中の電子がルテニウムに供与され、それが窒素分子に移動することで窒素三重結合(N≡N)の切断が容易となり、ルテニウム上で切断された水素はケージ内にH-イオンとして取り込まれ、原子状水素として放出され窒素原子と反応しアンモニアが生じます。
今回の成果により、穏和な条件でのアンモニア合成を実現するには、電子注入効果と水素吸蔵効果が重要な役割を果たしていることが明確になりました。従って、アンモニア合成プロセスの省エネルギー化に向けた触媒開発の有力な手がかりが得られたことになります。また、この触媒を用いると、安定な窒素分子の解離が速やかに進行することを利用できるため、アミンなど窒素を含む化合物を合成する化学反応への応用展開が期待されます。
用語説明
[用語1] エレクトライド : 電子がアニオンとして働く化合物の総称です。通常の物質の性質からは逸脱した性質を持つ物質として関心を集めていましたが、あまりに不安定なため、物性がほとんど不明のままでした。細野グループは、2003年に直径0.5ナノメートル程度のカゴ状の骨格が立体的につながった結晶構造をしている12CaO・7Al2O3を使って、安定なエレクトライドを初めて実現しました。このエレクトライドは金属のようによく電気を通し、低温では超伝導を示す。また、アルカリ金属と同じくらい電子を他に与える能力を持つにもかかわらず、化学的にも熱的にも安定というユニークな物性を持つ。
[用語2] 律速段階 : 化学反応において最も遅い反応段階であり、この反応速度が全体の化学反応の速度を支配している。
[用語3] 触媒 : 化学反応系に少量存在して、化学反応を著しく加速したり、特定の反応だけを起こしたりするが、それ自体は反応の前後で変化しない物質である。
[用語4] 同位体 : 原子番号が同じで、重さ(質量数)だけが異なる原子のことで、化学的性質は同等である。
[用語5] 活性化エネルギー : 反応の出発物質の基底状態から遷移状態に励起するのに必要なエネルギーのことであり、このエネルギーが小さいほど、その反応は容易になる。反応中に触媒が存在することで、活性化エネルギーを下げることが可能である。
[用語6] 速度論解析 : 化学反応の速度を解析することで、反応のメカニズムや化学反応の本質を明らかにするための解析手法である。
[用語7] 水素吸蔵特性 : 物質が、水素を物質内部に取り込む性質のことである。
論文情報
掲載誌 : |
Nature Communications |
論文タイトル : |
Electride support Boosts Nitrogen Dissociation over Ruthenium Catalyst and Shifts the Bottleneck in Ammonia Synthesis (エレクトライド担体がルテニウム触媒上での窒素切断を促進し、アンモニア合成の律速を変化させる) |
著者 : |
Masaaki Kitano, Shinji Kanbara, Yasunori Inoue, Navaratnarajah Kuganathan, Peter V. Sushko, Toshiharu Yokoyama, Michikazu Hara and Hideo Hosono
|
DOI : |
問い合わせ先
C12A7エレクトライドについて
東京工業大学 元素戦略センター センター長
応用セラミックス研究所 教授
細野 秀雄
Email : hosono@msl.titech.ac.jp
Tel : 045-924-5009
Fax : 045-924-5196
触媒反応について
東京工業大学 応用セラミックス研究所 教授
原 亨和
Email : mhara@msl.titech.ac.jp
Tel : 045-924-5311
Fax : 045-924-5381
JSTの事業に関すること
科学技術振興機構 戦略研究推進部 ACCELグループ
剱持 由起夫
Email : suishinf@jst.go.jp
Tel : 03-6380-9130
Fax : 03-3222-2066
報道担当
科学技術振興機構 広報課
Email : jstkoho@jst.go.jp
Tel : 03-5214-8404
Fax : 03-5214-8432
取材申し込み先
東京工業大学 広報センター
Email : media@jim.titech.ac.jp
Tel : 03-5734-2975
Fax : 03-5734-3661