東工大ニュース
東工大ニュース
公開日:2015.09.10
東京工業大学大学院生命理工学研究科の上野隆史教授と藤田健太大学院生らは、合成した分子のカゴをスイッチとした細胞内一酸化炭素(CO)放出システムの開発に成功した。具体的には、フェリチン[用語1]と呼ばれるカゴ状のたんぱく質の中に、COが結合した金属を閉じ込め、光を当てることによって、COがカゴから抜け出す仕組みを作り出した。
この手法を用いることにより、細胞内でCOを出すタイミングや量を自在に調節することが可能となった。また炎症抑制効果をもつたんぱく質NF-κB[用語2]の活性化とCOの関係を明らかにした。
今回の成果は、内閣府の最先端・次世代研究開発支援プログラムの支援によるもので、化学分野において最も権威のある学術誌の一つである「Angewandte Chemie International Edition(ドイツ化学会誌)」のオンライン版で9月2日にHot Paperとして公開された。
ヒトのからだは、体内に存在する様々なガス分子が伝達する信号によって保護されている。1998年に一酸化窒素ガスによる信号伝達機構についての研究がノーベル賞を受賞して以来、多くの研究者が、生体内でガス分子を扱う技術の開発に尽力している。
ガス分子の中でも特に一酸化炭素(CO)ガスは、生体内での取り扱いが難しい分子だったが、近年、金属カルボニル錯体と呼ばれる金属にCOが結合した分子からのCO放出反応を利用して、生体内へCOを輸送することが可能となり、COが抗炎症作用や細胞増殖などの細胞を保護する機能を持つことが徐々に明らかにされている。しかし実際には、COの放出のタイミングや量を人工的にコントロールすることが困難であったため、COが細胞内で伝達する信号を詳細に理解するには至っていなかった。
上野教授らは、光を当てたときにのみCOを放出させる性質を持つマンガンカルボニル錯体[用語3](図1a)の細胞内輸送に着目し、COの放出のタイミングや量をコントロールすることを目指した。カルボニル錯体は毒性や細胞内環境での不安定性が問題点とされるが、同教授らはこれまでに8ナノメートル(nm)の内部空間をもつカゴ状たんぱく質フェリチン(図1b)への内包によって改善されることを見出している。今回の研究においても、マンガンカルボニル錯体をフェリチンのカゴの中に集積させた複合体(図1c)で細胞内へ輸送することにした。

合成した複合体に光を照射し、CO放出実験を行ったところ、光刺激によって望んだタイミングでCOを放出できること、その放出量を光の照射時間によって変化させることができることが分かった(図2)。つまり、複合体は、光に応答するCO放出スイッチとしての機能を有しており、COの放出のタイミングや量を人工的に制御できる性質を持つことが明らかになった。
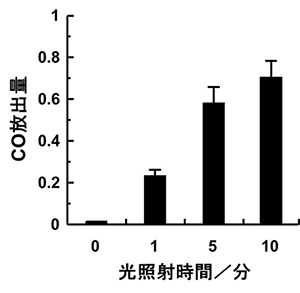
図2. 光照射時間に対するCO放出量の変化
NF-κBの活性化因子であるTNF-αと呼ばれる分子を添加したヒト胎児腎臓細胞(HEK293細胞)へ複合体を導入し、光を当てることによって、細胞内でのCO放出を誘導した。結果として、NF-κBを効率的に活性化させるには、1. 光照射によってCOが放出され、その信号が伝達された後に、2. NF-κBの活性化因子であるTNF-αの刺激が加えられることが重要であると分かった(図3)。
さらに、より多くのCOが放出されることもNF-κB活性化の向上に寄与していることを見出した。以上のCOの効果は、細胞内でCO放出スイッチとして機能する、今回合成したマンガンカルボニル錯体とフェリチンとの複合分子を用いることによってはじめて明らかにされた。
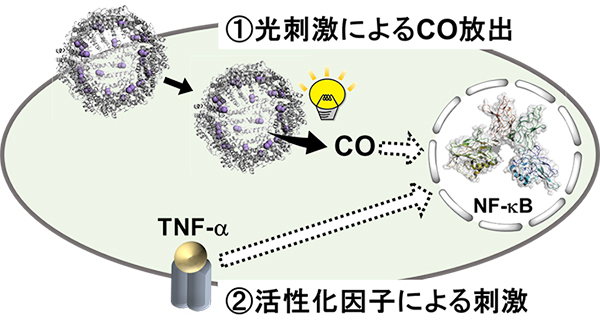
図3. 細胞内放出COによるNF-κB活性化機構
今回の研究では、COがTNF-αとNF-κBが関与する経路に着目したが、細胞内にはさらに様々な信号伝達経路が存在しており、今回、作製したスイッチを作動させるタイミングを調節することで、今後より詳細にCOの作用機構についての解明が進められていくと期待される。さらに、カゴ状たんぱく質を用いた細胞内で機能するスイッチの設計指針は、将来的にガスの放出以外の様々な化学反応を細胞内で進行させるために適用可能であると考えられる。
用語説明
[用語1] フェリチン : 24個の単量体から構成される外径8 nmのカゴ状のたんぱく質であり、天然では、そのカゴの内部に細胞内の鉄を貯蔵する役割を果たしている。近年、フェリチンのカゴを用いて、鉄以外の天然に存在しない金属化合物を集積させ、化学反応に利用する研究が進められている。
[用語2] 核転写因子NF-κB(エヌエフカッパービー) : 細胞内の核に存在する転写因子の一種。核内のDNAに結合することによって、標的となるたんぱく質の産生をコントロールする機能を有する。具体的には、抗炎症や抗アポトーシスなど、細胞を保護する役割をもつたんぱく質を標的としている。
[用語3] マンガンカルボニル錯体 : 一酸化炭素が結合した遷移金属錯体の一種。本研究で利用したマンガン型の錯体は光刺激によって一酸化炭素を放出するが、他の金属をもつ錯体では、光に対して安定なものも存在する。
論文情報
掲載誌 : |
Angewandte Chemie International Edition |
論文タイトル : |
A Photoactive Carbon-Monoxide-Releasing Protein Cage for Dose-Regulated Delivery in Living Cells |
著者 : |
Kenta Fujita, Dr. Yuya Tanaka, Dr. Satoshi Abe and Prof. Dr. Takafumi Ueno
|
DOI : |
問い合わせ先
大学院生命理工学研究科生体分子機能工学専攻
教授 上野隆史
Email : tueno@bio.titech.ac.jp
Tel : 045-924-5844 / Fax : 045-924-5806
東京工業大学 広報センター
Email : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661