東工大ニュース
東工大ニュース
公開日:2016.06.23
東京工業大学 科学技術創成研究院 化学生命科学研究所の吉田啓亮助教と久堀徹教授は、植物細胞内の機能制御に重要な還元力伝達経路として、これまで知られていたもののほかに、ニコチンアミドアデニンジヌクレオチドリン酸(NADPH[用語1])を起点とする経路が重要な役割を担っていることを発見した。
光合成の場である植物の葉緑体には、酸化力や還元力が酵素タンパク質に伝達され、タンパク質自体を酸化あるいは還元することによってその機能を調節するシステムがある。これまでは、光合成電子伝達系から電子を受け取るフェレドキシン[用語2]というタンパク質を起点とする還元力伝達経路がその主要経路であると考えられていた。吉田助教らは、これ以外にNADPHを起点とする還元力伝達経路が重要な役割を担っており、この二つの経路が協調して機能することが、植物の光合成や生育そのものに必須であることを明らかにした。
光合成反応は地球上最大の規模で行われる光エネルギー-化学エネルギー変換反応であり、植物による物質生産のかなめである。絶え間なく変動する自然環境の下で植物が効率よく安定して光合成反応を維持していくために、葉緑体の生理機能は柔軟に、そして精密に調節されている。
今回の研究成果は、この調節に重要な酸化力と還元力の伝達による葉緑体機能調節のネットワークを新たに解明したもので、光合成生物を用いた物質生産など、今後の応用研究への展開にも有効な重要な知見である。6月22日(現地時間)発行の「米国科学アカデミー紀要(Proc. Natl. Acad. Sci. USA)」電子版に掲載された。
植物の光合成は、光エネルギーを利用して炭水化物を生産する、いわば地球上のあらゆる生命を支える重要なエネルギー変換反応である。植物の緑葉の細胞の中には、葉緑体と呼ばれる細胞小器官があり、ここが光合成反応の場となっている(図1A)。個々の葉緑体の内部には、チラコイド膜とよばれる積層した生体膜があって、この膜に埋め込まれている光合成電子伝達系の働きによって光エネルギーが化学エネルギー(エネルギーを蓄積する化合物であるアデノシン三リン酸=ATPと、還元力を蓄える化合物であるNADPH)に変換されている。
次に、葉緑体の膜以外の部分(ストロマ)に存在する酵素群が働いて、大気中の二酸化炭素を原料として糖など炭水化物が生産されている。二酸化炭素を糖に変換する反応経路は、13種類の酵素が連続して働く複雑な反応で、発見者の名前を取って、Calvin-Benson(カルビン・ベンソン)回路とよばれている(図1B、2A)。Calvin-Benson回路が働くためには、上記のATPとNADPHが使われるが、この回路の酵素反応はいずれも光エネルギーを直接には必要としていない。そこで、以前はこの回路全体が“暗反応”と呼ばれ、明反応と呼ばれた電子伝達反応とは区別されていた。ところがその後の研究で、Calvin-Benson回路の少なくとも4つの酵素は光照射によって電子伝達系が働くとそれに連動して活性化される、ということがわかった。つまり、光を必要としないと考えられていた暗反応という定義が、実体に合わなくなってしまった。このため、暗反応、明反応という呼び名は使われなくなった。葉緑体内には、この“光照射のシグナル”をCalvin-Benson回路の酵素などに還元力として伝達し、葉緑体の機能全体を制御している還元力伝達経路がある。
このような還元力伝達経路は生物の細胞内に一般に見られるもので、系全体の酸化力あるいは還元力の蓄積レベルに応じて、特定の酵素が酸化されたり還元されたりするのを制御し、その酵素の活性を調節するシステムである。多くの場合、酵素は酸化されると活性を失い、還元されるとその活性が高くなる。このような制御システムで中心的に働いているのは、チオレドキシン[用語3]というタンパク質である。葉緑体では、光合成の電子伝達系から還元力を受け取ったチオレドキシンは、標的となる酵素に還元力を渡して、その酵素を活性型にする。そして、これまで30年以上、フェレドキシンからFTR[用語4]、チオレドキシンを介して標的酵素に到る単純な一本道の還元力伝達経路が制御システムとして働いていると考えられてきた(図2A)。
ところが、2000年に緑色植物であるシロイヌナズナの全ゲノムDNAの塩基配列が解読されて以来、植物細胞の中には、チオレドキシンやチオレドキシンに類似したタンパク質が合計20種類以上もあることがわかってきた。また、これらのタンパク質に還元力を伝達する上流の酵素も複数種類あることがわかった。さらに、チオレドキシンが還元力を渡す相手の酵素を解析する技術が発達し、葉緑体の中では実にさまざまな酵素がチオレドキシンから還元力を受け取っていることも報告されている。すなわち、葉緑体の還元力伝達経路は、これまで考えられていたような単純な一本道ではなく、複雑に分岐した“ネットワーク”によって構成されているらしいというわけである(図2B)。
イネのゲノム解析に基づいて、チオレドキシンの還元に関わるNADPH-チオレドキシン還元酵素(NTR)が2004年に3つ発見され、それぞれA,B,Cと命名された。このうち、3番目のNTRC[用語5]は、他の酵素と違った特徴を持っていた(図3)。このタンパク質は、植物細胞の細胞質にあるNTRと機能・構造が同じ部分とチオレドキシン部分が直列につながったハイブリッドタンパク質で、NADPHが蓄えた還元力を他の酵素に直接伝達することができるという、面白い葉緑体タンパク質だったのである。吉田助教らは緑色植物のNTRCの生化学・生理学的な特性を調べ、NTRCを通る還元力伝達経路とフェレドキシンを起点とする経路の違いを比較した。
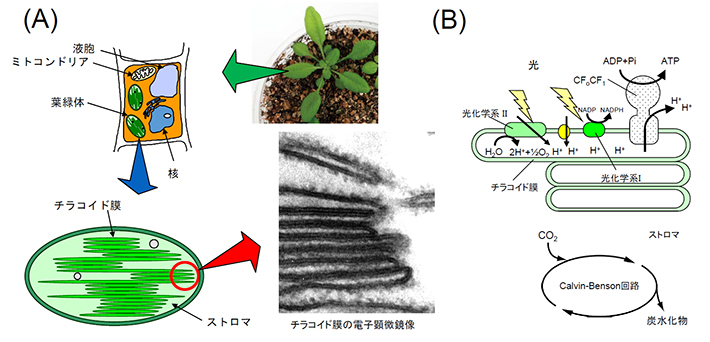
図1. 光合成の場である葉緑体の模式図
(A)植物の葉/細胞/葉緑体。チラコイド膜の電子顕微鏡写真は村上悟先生(東京大学名誉教授・故人)の提供による。
(B)葉緑体チラコイド膜の電子伝達系と葉緑体ストロマのCalvin-Benson回路の模式図。
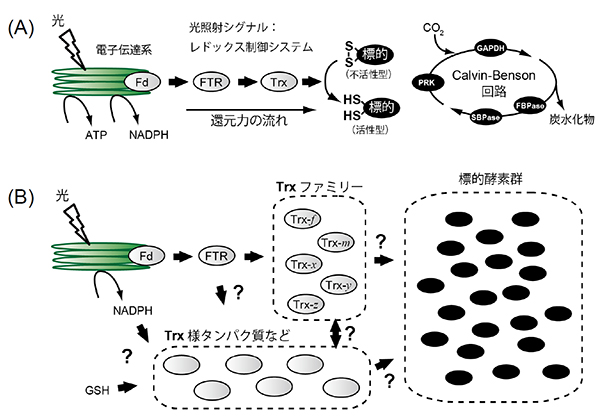
図2. 葉緑体の還元力伝達システムの模式図
(A)以前から知られていた葉緑体の還元力伝達システム。FTR/Trxシステムによる一本道の還元力伝達経路により、光照射のシグナルが還元力として標的酵素に伝達される。Calvin-Benson回路を構成する4つの酵素(GAPDH, FBPase, SBPase, PRK)は還元されて活性化される。
(B)新たに明らかになった葉緑体の還元力伝達ネットワーク。さまざまな還元力伝達因子(Trxファミリータンパク質やTrx様タンパク質など)といろいろな葉緑体の生理機能に関わる標的酵素によって構成されている。還元力経路をネットワーク状に組織化することによって、葉緑体機能は柔軟に、かつ、精密に調節されていると考えられる。
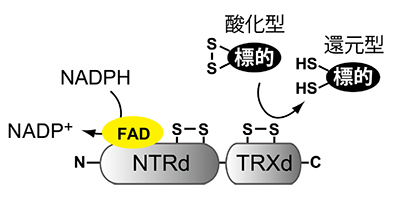
図3. NTRCの分子構造と反応の模式図
タンパク質のアミノ基末端側(図ではNと表示)にNADPH-チオレドキシン還元酵素部分(NTRd)、カルボキシル基末端側(図ではCと表示)にチオレドキシン部分(TRXd)を持つ。NTRdに結合したフラビンアデニンジヌクレオチド(FAD)がNADPHから還元力を受け取り、NTRdとTRXdがそれぞれ持っているふた組のシステインのペアに順次伝達する。そして、最終的に標的酵素が還元される。
吉田助教らは、まず、NTRCから還元力を受け取る可能性のあるタンパク質を調べるために、NTRCをクロマトグラフィー担体に固定し、葉緑体から抽出したタンパク質を結合相手のタンパク質群として用いてアフィニティークロマトグラフィー(生体物質を単離・精製する手法)を行った。その結果、すでにチオレドキシンの相手として報告されていたタンパク質のほか、NTRCが特異的に還元力を渡すタンパク質を見出した。さらに、この方法で見つかった相手のタンパク質について、NTRCから還元力がどのように伝達されるのかを試験管内で詳しく調べた。その結果、NTRCは、還元力の伝達速度や特異性の点で、これまで知られていたチオレドキシンとは異なる特長を持っていることを発見した(図4A)。
このNTRCの特長は、植物が生きる上でどのように重要なのだろうか。吉田助教らは、NTRCを欠損させた植物を育ててみたところ(図4B)、NTRCを欠損した植物の葉は、緑色にならなかった。そして、NTRCとFTRの両方を欠損させると、ほとんど育たなくなった。これらのタンパク質を欠損した植物の光合成効率などを調べてみると、NTRCを欠損させた植物では、光合成システムが全般的に機能不全に陥っているということがわかった。
これまで、葉緑体では光合成の電子伝達系が生み出す還元力を直接利用するFTRとチオレドキシンを経由する経路が、葉緑体の機能調節を行う唯一の還元力伝達経路である、というのが光合成研究分野の共通認識だった。しかし、今回の研究によって、葉緑体内ではNTRCも独自の機能を持っており、両者が協調して働くことが植物の葉緑体機能の調節にきわめて重要であるということがわかった。
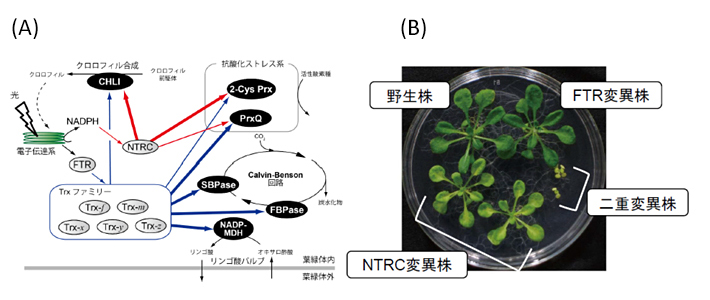
図4. FTR/Trx経路とNTRC経路はそれぞれ異なる還元力伝達経路によって協調的に葉緑体の機能調節と植物の生長を支える。
(A)TrxファミリーとNTRCの異なる標的選択性の模式図。還元力伝達効率の違いを矢印の太さで示した。赤矢印は、今回の研究で明らかになった経路。括弧内に各標的酵素が関与する生理機能を示している。
(B)シロイヌナズナのFTRとNTRC変異株、および、二重変異株。
葉緑体内の新しい還元力伝達経路の発見は、植物が進化の過程で獲得した環境応答戦略の新たな一面を明らかにしたものといえる。植物の機能制御に関わるこのような経路の発見は、将来、葉緑体の機能制御システムを人為的に改変・最適化することによって葉緑体機能を増強するなど、植物を利用した物質生産などの今後の応用研究にも役立つ重要な情報である。
この研究の主要部分は、現在、国立研究開発法人科学技術振興機構(JST)の戦略的創造研究推進事業チーム型研究(CREST)の久堀教授らの研究チームが取り組んでいるシアノバクテリアを用いた物質生産の基礎研究として実施された。また、研究の一部は、日本学術振興会科学研究費補助金・若手研究(B)(代表:吉田啓亮助教)と基盤研究(B)(代表:久堀徹教授)のサポートを受けている。
用語説明
[用語1] NADPとNADPH : ニコチンアミドアデニンジヌクレオチドリン酸(酸化型は正電荷を帯びるのでNADP+とも書く。還元型はNADPHと表記される)。葉緑体内では光合成の電子伝達系の還元力によってNADPHが生じるほか、ペントースリン酸回路のグルコース6-リン酸脱水素酵素の働きでも生産される。
[用語2] フェレドキシン(Fd) : 分子内に2Fe-2S型の鉄硫黄クラスターを持ち、還元力を鉄の価数の変化として分子内に貯めることが出来る。
[用語3] チオレドキシン(Trx) : 生体内の還元力伝達に中心的な役割を果たすタンパク質。生物界に普遍的に存在し、Trp-Cys-Gly-Pro-Cysというよく保存されたアミノ酸配列の活性部位モチーフを持っており、この二つのCys(システイン)のチオール基の酸化還元状態の変化によって還元力の伝達を行う。
[用語4] フェレドキシン/チオレドキシン還元酵素(FTR) : 電子伝達タンパク質であるフェレドキシンからチオレドキシンに還元力を受け渡す還元力伝達タンパク質。
[用語5] NADPH-チオレドキシン還元酵素C(NTRC) : 2004年、Serrato A. J.らによって報告された新規のNADPH依存的に標的酵素を還元する還元力伝達タンパク質(J. Biol. Chem. (2004) 279, 43821-43827)。その後、植物葉緑体やシアノバクテリアなど、光合成生物が特異的に持っていることがわかった。
論文情報
論文タイトル : |
Two distinct redox cascades cooperatively regulate chloroplast functions and sustain plant viability |
著者 : |
Keisuke Yoshida, Toru Hisabori |
掲載誌 : |
Proc. Natl. Acad. Sci. USA 2016, in press |
DOI : |
問い合わせ先
科学技術創成研究院 化学生命科学研究所
助教 吉田啓亮
Tel : 045-924-5267 / Fax : 045-924-5268
科学技術創成研究院 化学生命科学研究所
教授 久堀徹
Email : thisabor@res.titech.ac.jp
Tel : 045-924-5234 / Fax : 045-924-5268
取材申し込み先
東京工業大学 広報センター
Email : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661