東工大ニュース
東工大ニュース
公開日:2017.12.05
相同組換えのDNA鎖交換の素過程を世界で初めて解明 ―Rad51のDNA鎖交換反応は3ステップで進行する―
東京工業大学 科学技術創成研究院の伊藤健太郎研究員、岩崎博史教授、同生命理工学院のTakahashi Masayuki教授、国立遺伝学研究所の村山泰斗准教授(研究当時・東工大助教)の研究グループは、相同組換えにおけるDNA鎖交換反応の解明に世界で初めて成功した。
相同組換えは、遺伝情報の維持や遺伝的多様性を生み出すのに必須な反応であり、全ての生物で保存されている。相同組換えにおける中心的な反応は、似た配列を持つ(このことを“相同”という)2組のDNA間の鎖の交換反応である。DNA鎖交換反応は、Rad51リコンビナーゼ[用語1]によって触媒されるが、反応がどのように進行するのか不明だった。
今回の研究では、蛍光標識したDNAで鎖交換反応をリアルタイムにモニターして解析を行った。その結果、鎖交換反応は連続した3ステップ反応で進行することを発見した。さらに、Rad51の低分子補助因子であるATP[用語2]やタンパク質性補助因子であるSwi5-Sfr1タンパク質複合体[用語3]の役割を明らかにした。
この成果は、2017年12月4日のNature Structural and Molecular Biology電子版に掲載された。
今回、DNA鎖を蛍光標識し、蛍光共鳴エネルギー移動(Fluorescence resonance energy transfer: FRET)[用語4]の原理を利用することで、DNA鎖交換反応の反応中間体形成と最終産物生成をそれぞれリアルタイムで観察する2種類の分析方法(アッセイ系)を構築した。このアッセイ系を用いることで、極めて複雑な反応のため正確なアプローチが困難であったRad51によるDNA鎖交換反応を解析した。その結果、次の3つのステップを経て、この交換反応が進行することを発見した。
これは、1)一本鎖DNAに数珠状に結合したRad51リコンビナーゼが鎖交換相手となるDNAの相同な配列を見つけて、最初の反応複合体(C1反応中間体)を形成する、2)C1反応中間体が変化し、次の反応中間体C2ができる、3)C2反応中間体が解消されて反応が完了するという3つのステップである。
Rad51によるDNA鎖交換反応には低分子補助因子ATPが必要であるが、これまでその役割が不明であった。今回、最初のC1反応中間体を形成する際にはRad51がATPと結合する必要があること、そして、ステップが進みC1→C2遷移や最終産物生成時にはATPが加水分解されることが必須であることがわかった(但し、ある条件ではC1→C2遷移時にATP加水分解は必要ないことも判明したが、最終産物生成するにはどの条件でもATP加水分解が必須)。また、Rad51補助因子であるSwi5-Sfr1複合体は、リコンビナーゼによるATP加水分解を伴って、C1→C2遷移と最終産物生成のステップを促進することが明らかになった(図1)。
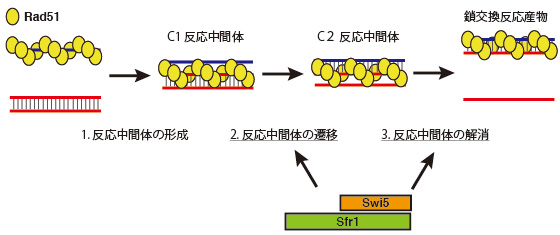
図1. Swi5-Sfr1複合体によるDNA鎖交換反応の促進モデル
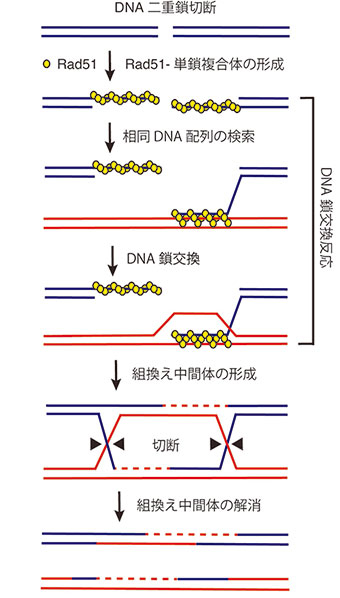
図2. 相同組換えによるDNA二重鎖切断の修復モデル
紫外線や放射線などの外的要因、DNA複製の阻害や代謝で発生した活性酸素などの内的要因により、DNAは日常的に様々な種類の損傷を受けている。DNAの二重鎖が切断された損傷(DNA二重鎖切断)は特に重篤な損傷で、修復されなければ細胞死の原因となり、間違った修復が行われるとがんの原因となりうる。
相同組換えは、遺伝的多様性を生み出すのに必須な反応であるが、DNA二重鎖切断を正確に修復する機構(組換えによるDNA修復機構、組換え修復といわれている)としても極めて重要な働きをしている。例えば、マウスでは、RAD51遺伝子を欠損すると死んでしまうことから、その重要性が実証されている。実際、全ての生物種が相同組換え機構を持っており、この機構は生命に必須の普遍的な生理機能である。
相同組換えは多段階で起こる極めて複雑な反応であり、DNA複製や転写などといった他の核内現象に比べるとその仕組みの解明は遅れている。相同組換えの中心的な反応はDNA鎖交換反応であり、Rad51リコンビナーゼによって触媒される(図2)。Rad51リコンビナーゼは、一本鎖DNAに数珠状に結合しDNA鎖交換反応の開始前複合体を形成する。その後、開始前複合体は、鎖を交換する相手となる二重鎖DNAの相同な配列を探し、相同鎖が見つかるとDNA鎖の交換を行う。
RAD51遺伝子は、大阪大学のグループによって1992年に出芽酵母から発見され、その後、ヒトを含めて多くの生物種で見つかっている。これまでRad51タンパク質のDNA鎖交換活性について世界中で様々な解析がなされてきた。2003年に、岩崎教授の研究グループは、分裂酵母を用いた研究からSwi5-Sfr1タンパク質複合体がRad51の補助因子であることを発見し、その後継続してSwi5-Sfr1複合体によるRad51の活性制御機構について解析を続けてきた。これまで多くの研究者がRad51によるDNA鎖交換反応の進行過程を明らかにしようとしていたが、今回FRETを用いたリアルタイムのアッセイ系でその進行過程の観察に世界で初めて成功した。
マウスにおいてRAD51遺伝子を欠損すると死んでしまうことから、生命にとって組換えや組換え修復が極めて重要な働きをしていることがわかる。RAD51の補助因子にはSwi5-Sfr1複合体の他にも様々なものが知られている。有名なものでは、BRCA2タンパク質がある。BRCA2遺伝子の欠損や突然変異は致死とはならないが、家族性乳がんの原因となることが知られている。これは、致死と比べれば軽度な表現型であるといえるが、組換え修復不全が発がんの原因になるということを直接的に示している例である。すなわち、これは正常な組換え(修復)機能がゲノムの安定性を維持しガンを抑制していることを示す一つの典型例である。
今回確立したアッセイ系を用いて、BRCA2タンパク質によるRAD51活性制御機構の詳細が解析されると、細胞内で相同組換えを正しく進行させる仕組みの理解が大きく進展する。このような詳細な基礎研究を基盤として、今後、発がんやがん抑制の詳細な仕組みが明らかにされていくと考えられる。
用語説明
[用語1] Rad51リコンビナーゼ : 相同組換えの中心的な反応であるDNA鎖交換反応を触媒するタンパク質。酵母などの単細胞真核生物からヒトまで、すべての真核生物に存在する。バクテリアのRecAタンパク質と相似タンパク質である。Rad51やRecAタンパク質は、ATP存在下で一本鎖DNA上に右巻らせん状に巻き付き、このタンパク質核酸複合体(開始前複合体)は相手となる二重鎖DNAの相同性を検索し、相同性が見つかればDNA鎖の交換反応を推進する。
[用語2] ATP : アデノシン三リン酸(adenosine triphosphate)。生体内に広く存在し、3位にリン酸が結合したり解離したりすることで、エネルギーの放出や貯蔵、代謝や合成に重要な役目を果たしている。その重要性からエネルギーの通貨と形容されている。ある種のタンパク質や酵素は、ATPとの結合やATPを加水分解することで、構造変化を引き起こし、その機能を発揮することが知られている。
[用語3] Swi5-Sfr1タンパク質複合体 : Rad51の鎖交換反応を促進する補助因子の1つ。2003年、分裂酵母で最初に見つかった。Rad51の鎖交換反応を促進したり抑制したりするタンパク質は、これ以外にも複数知られている。これら複数のタンパク質複合体によってRad51によるDNA鎖交換活性は精緻に制御されているが、まだ、その全容は解明されていない。
[用語4] 蛍光共鳴エネルギー移動 (Fluorescence resonance energy transfer: FRET) : 2つの蛍光分子が近接して存在している時、供与体となる蛍光分子から受容体となる蛍光分子へ励起エネルギーが直接移動する現象。今回の実験では、受容体が近くにあると遠くにある場合に比べて、励起した供与体から発する蛍光強度が低下することを利用している。すなわち、1)Rad51と結合した一本鎖DNA(供与体蛍光分子を付加してある)と相同な二重鎖(受容体蛍光分子を付加してある)が複合体を形成した際にFRETが起こり、その結果、供与体の蛍光強度の低下が起こる現象と、2)鎖交換の末に元の二重鎖(供与体と受容体を付加してあり、FRETが起こっている)が引きはがされて一本鎖DNAになることでFRETから解放されて供与体の蛍光強度が上昇する現象を利用した。今回の研究では、これらの蛍光変化をリアルタイムで観測する2種類のアッセイ系を構築し、鎖交換反応の素過程を解析した。
論文情報
掲載誌 : |
Nature Structural and Molecular Biology |
論文タイトル : |
Two three-strand intermediates are processed during Rad51-driven DNA strand exchange |
著者 : |
Kentaro Ito, Yasuto Murayama, Masayuki Takahashi, and Hiroshi Iwasaki |
DOI : |
お問い合わせ先
東京工業大学 科学技術創成研究院
細胞制御工学研究センター
岩崎博史 教授
E-mail : hiwasaki@bio.titech.ac.jp
Tel : 03-5734-2588 / Fax : 03-5734-3781
取材申し込み先
東京工業大学 広報・社会連携本部 広報・地域連携部門
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661