東工大ニュース
東工大ニュース
公開日:2019.11.18
東京工業大学 科学技術創成研究院 先導原子力研究所の島田幹男助教、松本義久准教授、環境・社会理工学院 融合理工学系 原子核工学コースの塚田海馬大学院生、香川望大学院生(当時)の研究グループはヒト皮膚由来線維芽細胞[用語1]からiPS細胞[用語2]を作成し、iPS細胞の放射線応答に関する遺伝子発現[用語3]の変化を明らかにした。
ヒト初代継代線維芽細胞からiPS細胞を作成、神経幹細胞に分化誘導し、細胞に対して放射線照射後、次世代シークエンサーによるRNAシークエンス技術[用語4]により、それぞれの細胞の遺伝子発現変化を解析。その結果、iPS細胞では通常の体細胞と比較してDNA修復や細胞周期チェックポイントなどゲノムDNAを守る仕組みが強くなり、一方である程度DNAに損傷を持つ細胞は積極的に細胞死によって排除される傾向があることを見出した。
ヒトの体細胞からiPS細胞へと変化させる技術はリプログラミングと呼ばれ、ヒトの臓器移植や疾患の治療などの再生医療分野で期待されている。一方で細胞内のゲノムDNA[用語5]は細胞内外からの様々な刺激により常に損傷を受けているため、これらを修復する分子機構が存在するが、iPS細胞におけるDNA修復の分子メカニズムは不明な点が多かった。
研究成果はOxford Journal(オックスフォードジャーナル)出版社による日本放射線影響学会の学会誌「Journal of Radiation Research」(オンライン版)で10月28日に公開された。
ヒトをはじめとした生物の細胞のゲノムDNAは常時、紫外線や放射線といった細胞内外からの刺激により損傷を受けている。DNAの損傷は突然変異や細胞のがん化の原因となるために直ちに修復されなければならない。このため細胞にはDNA修復機構が備わっており、ゲノムDNAを守っている。
一方でiPS細胞は様々な細胞に変化する能力を持ち、臓器再生や疾患治療などへの応用が期待されるが、同時にiPS細胞自身ががん化する懸念が残っており、がん化するメカニズムの解明が急務となっている。一般的に細胞のがん化の原因はDNAに生じた「傷」が原因であり、通常はDNA修復機構により修復されるが、iPS細胞におけるDNA修復機構の制御機構は不明だった。そこでiPS細胞におけるDNA修復機構などDNAを守る分子の仕組み解明を試みた。
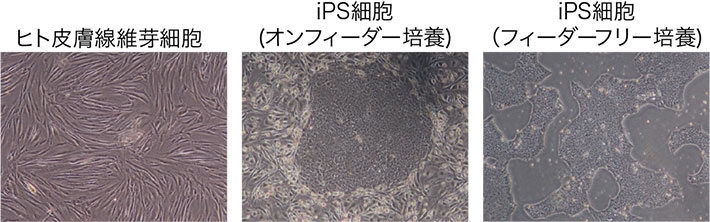
図1. 今回の研究で用いた細胞の明視野顕微鏡像
左がヒト皮膚由来の線維芽細胞、中央がマウスの胎児線維芽細胞上で培養している(オンフィーダー培養)iPS細胞、右がiPS細胞のみで培養している様子。
研究グループはヒト線維芽細胞からiPS細胞を樹立し、ゲノム安定性に関与する遺伝子グループの発現解析を実施。またiPS細胞から神経幹細胞を樹立することにより皮膚線維芽細胞→iPS細胞→神経幹細胞といった細胞の分化による遺伝子発現の変化も同時に解析した。
まず、細胞に放射線(ガンマ線)を5 Gy(グレイ)照射、1時間後に細胞からRNAを抽出し、次世代シークエンサーを用いて遺伝子発現を比較した。その結果、線維芽細胞からiPS細胞へと初期化[用語6]することにより、DNA修復、細胞周期チェックポイントといった遺伝子を正常に保つための分子の発現が高くなっていることがわかった。
一方、アポトーシスという細胞死に関する遺伝子発現も高くなっていたことから、ある程度のDNA損傷を持つ細胞は積極的に細胞死によって排除されることもわかった。特に興味深いのはCDKN1A[用語7]という遺伝子はp21というタンパク質を産生するが、iPS細胞ではこの発現量が大幅に低下していた。 p21はDNAに傷が生じた際に細胞分裂の周期を一度停止して、DNA修復にかかる時間を維持する役割を持つが、p21が少ないということは細胞周期を停止しないということを示している。すなわち、細胞分裂の周期を停止しなくても修復できる程度の損傷の場合はすぐに修復し、ある一定の閾値を超える損傷の場合はアポトーシスにより細胞死を起こすことが考えられる。
また、放射線の照射の有無によって遺伝子発現が増加する場合も確かめられたがこれらの傾向はiPS細胞特異的というよりは通常の細胞とよく似た傾向であった。
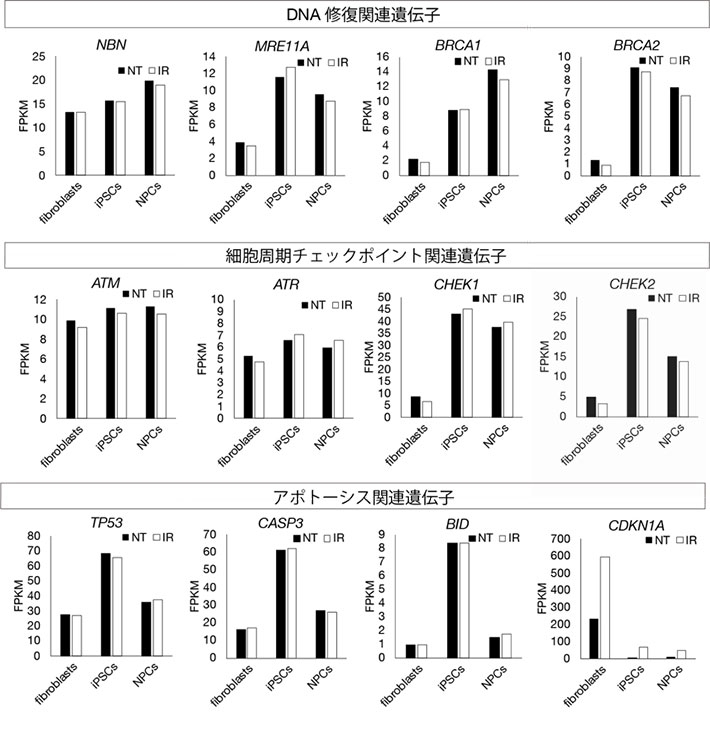
図2. iPS細胞におけるゲノム安定性関連遺伝子の発現変化
ヒト皮膚線維芽細胞(fibroblasts)、iPS細胞、神経幹/前駆細胞(NPCs)に放射線を照射(IR ガンマ線5 Gy照射1時間後)および非照射(NT)の細胞からRNAを抽出し次世代シークエンサーで解析した結果。縦軸は FPKMで遺伝子発現量の比を表す。iPS細胞ではDNA修復、細胞周期チェックポイント、アポトーシスに関係する遺伝子全てで発現量が増加していることがわかる。一方で、神経幹細胞に分化させると、発現量が増加する場合と、減少する場合で分かれる。これはそれぞれ神経系で必要な遺伝子かどうかを示しており、神経発生との関連が考えられる。
iPS細胞は多能性幹細胞という様々な臓器に変化することができる細胞の一種であり、遺伝子の設計図であるゲノムDNAがより安定に維持されていなければならない。今回の研究成果によりiPS細胞が遺伝子発現制御を通じて巧みにゲノムDNAの安定性を維持し、それが困難だと判断した場合は即座に細胞死により排除するメカニズムが明らかになった。
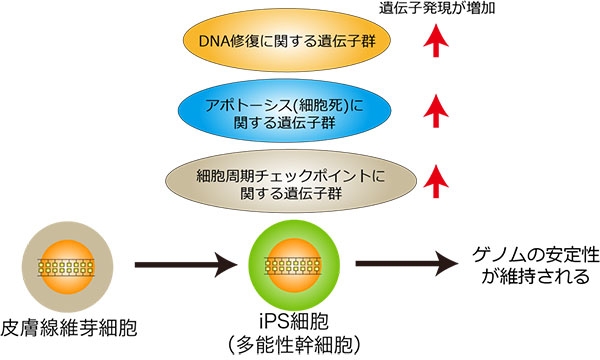
図3. 今回明らかになった研究結果
iPS細胞は初期化した後、ゲノム安定性に関与する遺伝子発現を増加させることにより、ゲノムの安定性を維持することが明らかになった。
今回研究グループはiPS細胞における網羅的な遺伝子発現解析により放射線や紫外線から体を守る遺伝子調節の仕組みを明らかにした。今後は、分子生物学的なアプローチによってそれぞれの遺伝子の機能を明らかにし、再生医療への貢献や放射線防護の発展に貢献することが期待される。
用語説明
[用語1] 皮膚線維芽細胞 : 皮膚細胞から採取した線維芽細胞。結合組織を構成する代表的な細胞で、皮膚が損傷した際などに細胞分裂し、治癒に貢献する。
[用語2] iPS細胞(Induced Pluripotent Stem Cells) : 体細胞から樹立可能な多能性幹細胞。様々な組織の細胞に分化することが可能である。
[用語3] 遺伝子発現 : 細胞の遺伝子はゲノムDNAに保存されているが、実際にはRNAを経てタンパク質に変換されないと機能しない。細胞は必要に応じて遺伝子をタンパク質に変換して機能しており、それを遺伝子発現という。
[用語4] RNAシークエンス技術 : 次世代シークエンサーを用いて細胞内に発現している遺伝子量を網羅的に解析することができる技術。
[用語5] ゲノムDNA : 細胞内で遺伝子情報がコードされているDNA。
[用語6] 初期化 : 体細胞からiPS細胞を樹立する際に、遺伝子発現やクロマチン制御の状態が個体発生の初期状態の戻るために初期化という。
[用語7] CDKN1A : p21というタンパク質をコードしている遺伝子。p21は細胞周期停止を促進するタンパク質で、細胞のがん化や老化などと深い関わりを持つ。
論文情報
掲載誌 : |
Journal of Radiation Research |
論文タイトル : |
Reprogramming and differentiation-dependent transcriptional alteration of DNA damage response and apoptosis genes in human induced pluripotent stem cells |
著者 : |
Mikio Shimada, Kaima Tsukada, Nozomi Kagawa, Yoshihisa Matsumoto |
DOI : |
お問い合わせ先
東京工業大学 科学技術創成研究院 先導原子力研究所
助教 島田幹男
E-mail : mshimada@lane.iir.titech.ac.jp
Tel : 03-5734-3703 / Fax : 03-5734-3703
取材申し込み先
東京工業大学 広報・社会連携本部 広報・地域連携部門
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661