東工大ニュース
東工大ニュース
公開日:2021.03.23
東京工業大学 生命理工学院 生命理工学系のチャン・フ・ズイ助教、北尾彰朗教授、理化学研究所 革新知能統合研究センターのアドナン・スリオカ研究員、トロント大学のスコット・プロッサー教授、カリフォルニア大学サンディエゴ校のロジャー・スナハラ教授らの国際共同研究チームは、フッ素19核磁気共鳴法[用語1]、分子動力学シミュレーション[用語2]、数理剛性理論[用語3]を組み合わせることで、ヒトのアデノシンA2A受容体(A2AR)の活性化の鍵となる仕組みを明らかにした。
A2ARは、Gタンパク質と結合して細胞のシグナル伝達を開始する機能を持つGタンパク質共役型受容体(GPCR)の一種である。がんや動脈硬化など様々な薬のターゲット分子として有用だが、薬理学的現象に重要であるGタンパク質活性化のプロセスはこれまで十分明らかになっていなかった。本研究では、核磁気共鳴法によって、A2ARには少なくとも2つの不活性状態と3つの活性状態が同時に存在しており、その共存比率がリガンド[用語4]の結合やGタンパク質の活性化状態に依存して変化することを明らかにした。また、分子動力学で得られたA2ARとGタンパク質の複合体立体構造を数理剛性理論で解析することで、A2ARのリガンド結合部位からGタンパク質へ長距離の情報伝達経路を特定できた。本研究でA2ARの活性化の鍵となる仕組みを解明できたことで、A2ARに作用する新たな薬剤の開発につながると期待される。
本研究成果は、2021年3月19日付の科学誌「Cell(セル)」オンライン版に公開され、同誌4月号に掲載される。
Gタンパク質共役型受容体(GPCR)は、活性化すると細胞内のGタンパク質と結合して、シグナル伝達を開始する機能を持つ。GPCRに分類される膜タンパク質には多くの種類があるが、GPCRは薬剤が結合するターゲット分子として有用であり、承認されている全医薬品の35%はGPCRに作用する。これは、GPCRの大半が細胞膜に存在しており、GPCRに作用する薬剤やリガンドは細胞外ポケットに結合することから、多くの場合、薬物が細胞内に入らなくても作用できるというメリットがあるためである。
多くの薬理学的現象では、GPCRにリガンドが結合してからGタンパク質が活性化されるまでの間に生じる立体構造変化などの動的な事象や中間状態が重要な役割を果たしている。ただし、GPCRの構造ダイナミクスや、活性化やシグナル伝達における中間状態とその役割はこれまで必ずしも明確になっておらず、GPCRの活性化メカニズムの理解を深めるための重要な課題とされてきた。
国際共同研究チームはこの課題に取り組むために、Gタンパク質共役型受容体(GPCR)としてよく知られているヒトのアデノシンA2A受容体(A2AR)(図1)を、なるべく天然に近い環境で研究することを目指した。A2ARは、カフェインなどのリガンド分子によって不活性化されることからカフェイン受容体としても知られているが、Gタンパク質と結合して細胞のシグナル伝達を開始させる。
この研究を実施するために、脂質ナノディスクに受容体を組み込んで再構成し、フッ素核磁気共鳴法を利用することで、生理学的なプロセスを確認できる環境下でA2ARが取りうる複数の状態間の平衡を調べる方法を開発した。核磁気共鳴法では、活性化プロセスにおいて重要な中間体を同定することができ、またマイクロ秒から数秒にわたって立体構造のダイナミクスの情報を得ることができる。このフッ素19核磁気共鳴法に、分子動力学シミュレーションと、アドナン・スリオカ研究員が開発した数理剛性理論を組み合わせることで、A2ARの立体構造ダイナミクスとシグナル伝達の包括的な検討が可能になった。
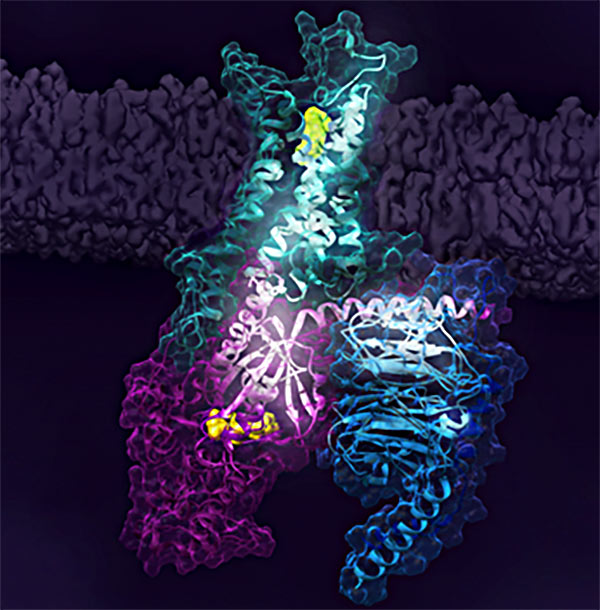
図1. A2ARからGタンパク質へと至る活性化の情報伝達経路
リガンド(上部の黄緑色の部分)の結合によって活性化されたヒトA2Aアデノシン受容体(明青緑色)は、Gタンパク質三量体Gαβγ(紫、淡青、濃青)へと活性シグナルを伝達する。活性経路はクレオチド結合部位(黄色)まで延びている。
国際共同研究チームは、フッ素19核磁気共鳴法、数理剛性理論、分子動力学シミュレーションを用いて、A2AR活性化の鍵となる仕組みを明らかにした。
まず、フッ素19核磁気共鳴法によってA2ARへのGタンパク質やリガンドの結合によるNMRスペクトルの変化を調べた。その結果、A2ARには、少なくとも2つの不活性状態と3つの活性状態が同時に存在しており、その共存比率がリガンドの結合やGタンパク質の活性化状態に依存して変化することがわかった(図2)。
次に、分子動力学シミュレーションで得られたA2ARとGタンパク質の複合体立体構造を数理剛性理論で解析することで、A2ARのリガンド結合部位からGタンパク質へ長距離の情報伝達経路を特定した(図3)。特に、Gタンパク質のGβγサブユニットがシグナル伝達と受容体の完全な活性化に重要であることが明らかになった。
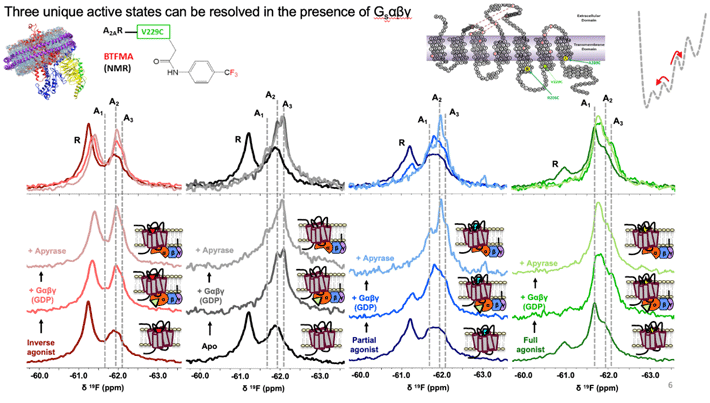
図2. フッ素19核磁気共鳴法による複数の状態の共存比率の変化
NMRスペクトルから、少なくとも3つの活性な構造状態(A1、A2、A3)、および不活性状態(R)を識別できる。Gタンパク質が結合すると活性状態の比率が増大し、さらにリガンドが結合すると、A1状態が顕著になる。
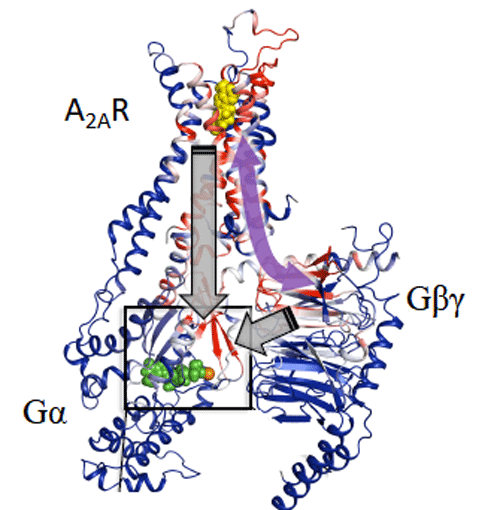
図3. 分子動力学シミュレーションで得られたA2ARとGタンパク質の複合体立体構造
更に数理剛性理論による解析で、リガンド(黄色)が結合したA2ARと、ヌクレオチド(緑色)が結合したGタンパク質GαとGβγの間を結ぶ活性化ネットワーク経路(矢印)が見つかった。
今回の研究では、A2ARの立体構造変化や中間状態などを調べることで、活性化の鍵となる仕組みを明らかにすることができた。
A2ARに作用する薬はすでに、炎症やがんに加えて創傷治癒や、動脈硬化、再狭窄、血小板活性化などに対応するものが開発されている。A2ARのシグナル伝達に関連した機能的状態を理解することは、新たな創薬の機会につながると期待できる。
今後の研究では、A2ARの別の部位に焦点を当てることで、活性化プロセスのより包括的な描像を得ることを目指している。
付記
本研究は、以下の事業・研究領域・研究課題などの支援を受けて行われた。
用語説明
[用語1] フッ素19核磁気共鳴法 : 注目する部位に結合させたフッ素19(安定同位体)から生じる核スピンの共鳴現象の信号を磁場の中で測定し、分子構造や物性を測定する手法。
[用語2] 分子動力学シミュレーション : 対象とするシステムを原子の集合体としてコンピュータ上でモデル化し、運動方程式を数値的に解くことで原子の位置や速度の時間的変化を計算するシミュレーション法。
[用語3] 数理剛性理論 : 例えば、二次元平面において□の形に組まれた枠組みは、力を加えて変形させることができるが、もう一本加えて〼にすると変形できない剛体になる。このような性質を数理的に解析する理論を数理剛性理論という。
[用語4] リガンド : 受容体タンパク質などの特定の生体分子に結合し、何らかの影響を及ぼす分子のことをいう。
論文情報
掲載誌 : |
Cell |
論文タイトル : |
Delineating the conformational landscape of the adenosine A2A receptor during G protein coupling |
著者 : |
Shuya Kate Huang, Aditya Pandey, Duy Phuoc Tran, Nicolas L. Villanueva, Akio Kitao, Roger K. Sunahara, Adnan Sljoka, and R. Scott Prosser |
DOI : |
お問い合わせ先
東京工業大学 生命理工学院
教授 北尾彰朗
E-mail : kitao.a.aa@m.titech.ac.jp
Tel : 03-5734-3373 / Fax : 03-5734-3372
JST事業に関すること
科学技術振興機構 戦略研究推進部ICTグループ
舘澤博子
E-mail : crest@jst.go.jp
Tel : 03-3512-3526 / Fax : 03-3222-2066
取材申し込み先
東京工業大学 総務部 広報課
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661
理化学研究所 広報室 報道担当
E-mail : ex-press@riken.jp
科学技術振興機構 広報課
E-mail : jstkoho@jst.go.jp
Tel : 03-5214-8404 / Fax : 03-5214-8432