東工大ニュース
東工大ニュース
公開日:2019.07.05
東京工業大学 科学技術創成研究院 化学生命科学研究所の杉浦一徳研究員(研究当時。現職 大阪大学 産業科学研究所 生体分子機能科学研究分野 特任研究員)と久堀徹教授らは緑色植物葉緑体内の酸化還元制御機構[用語1]の鍵タンパク質であるチオレドキシン[用語2]の酸化還元状態をリアルタイムにモニターできる蛍光タンパク質センサーCROST(Change in redox state of thioredoxin)[用語3]を開発し、明暗条件の変化により植物体内でチオレドキシンの酸化還元が変化する様子を捉えることに成功した。
チオレドキシンが光合成の電子伝達系から還元力を受け取ると、分子表面の2個のシステインのチオール基[用語4]が還元状態になる。還元型チオレドキシンが葉緑体内の様々な酵素分子を標的として働き、酵素分子が持っているジスルフィド結合[用語5]を還元する。還元された酵素分子は構造変化を起こし、通常活性型になる。こうしてチオレドキシンは光合成が始まるのに対応して、葉緑体内の様々な酵素分子の活性を制御する因子として働く。このため、チオレドキシンがいつどのくらい還元されるかを調べることは、葉緑体の機能制御のメカニズムを探る大切な情報となる。
これまでチオレドキシンの状態を調べるには、葉を瞬間凍結して組織の中のタンパク質分子の状態を化学的に調べる方法が一般的だった。しかし、電子移動は瞬時に起こるため、タンパク質の細胞内の動態を探るにはリアルタイムに酸化や還元状態を探る方法が不可欠だった。
研究成果は6月20日付け、アメリカ分子生物学生化学会誌「Journal of Biological Chemistry(バイオロジカル・ケミストリー)」に掲載された。
チオレドキシンは生体内の酸化還元状態を利用して様々な生体分子を調節する非常に重要なタンパク質で、動植物、細菌などほとんど全ての生物が持っている。中でも、植物の光合成の場である葉緑体に局在しているチオレドキシンは、光合成反応の調節を行う重要な役割を担っていることが知られている。
光合成では、光エネルギーを化学エネルギーに変換する重要なエネルギー変換プロセス(光エネルギー変換過程)と、二酸化炭素を有機物に変換する化学合成プロセスとを協調的に働かせるために、酵素の活性をうまくコントロールすることが不可欠となる。そのために植物が獲得した方法が、光エネルギー変換過程で水の分解によって生じる還元力そのものを利用して、タンパク質を還元して活性調節するという方法である。この時に生じる多くの還元力は二酸化炭素の還元に用いられ、糖が合成されるが、チオレドキシンは一部の還元力をこの糖の合成を触媒している酵素分子そのものの還元に利用し、その活性を調節する。
したがって、植物体内ではチオレドキシンの酸化還元状態が、植物の機能制御を理解するうえで欠かせない重要な情報といえる。これまで、チオレドキシンの酸化還元状態を調べる方法は化学修飾によるものが一般的で、リアルタイムにタンパク質の状態を観察する方法はなかった。
葉緑体内には、チオレドキシンによって還元されることで大きく構造が変化するCP12というタンパク質がある。CP12は還元状態では伸びた構造と考えられているが、分子内に二組のジスルフィド結合を形成することができるため、酸化されるとこのジスルフィド結合によって分子の形が大きく変わると予想される。杉浦研究員らはこの性質に着目し、チオレドキシンの酸化還元状態の変化を検出できないかと考えた。
今回開発した蛍光タンパク質センサーCROSTは、このCP12の一部を切り取って二つの蛍光タンパク質の間に挟み込んだものである。まずCP12の半分を利用して酸化還元で構造が変化するタンパク質部品を作り、この部品の両側に長波長側に蛍光を発するYFP[用語6]と短波長側に蛍光を発するCFPをそれぞれ結合する。この融合分子では、CP12断片の酸化還元状態が変化するとYFPとCFPの分子間距離が変わり、酸化還元状態の変化を蛍光のエネルギー共鳴移動効率の変化として検出することができる(図1、図2)。CP12部分の酸化還元は、チオレドキシンの酸化還元状態の変化に呼応して速やかに起こるので、CROSTを用いることでチオレドキシンの酸化還元状態を蛍光測定によってモニターすることが可能になった。
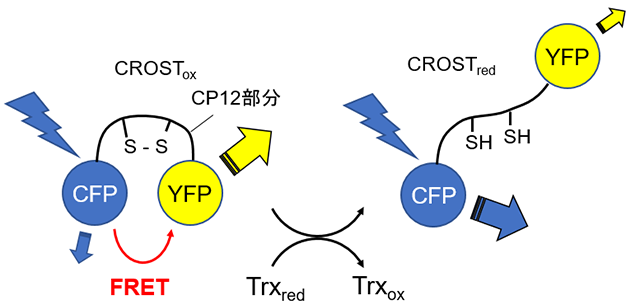
図1. 開発したチオレドキシン酸化還元センサーの酸化還元による構造変化
このCROST分子を実際に緑色植物シロイヌナズナの葉の葉緑体内に発現して明暗条件を変えると、光のオンオフによってCROST分子に由来する蛍光の変化を捉えることに成功した(図3)。この変化は、光が当たると葉緑体内でチオレドキシンが還元され、暗所に戻すと酸化されることに対応している。
このセンサーの開発によって、植物の葉緑体内がどのような環境の時にチオレドキシンが還元され、酵素分子の活性化が起こるのかを経時的に調べることが可能になった。今後は、光だけでなく様々な環境の変化に対して、葉緑体の代謝系酵素の活性制御を行うチオレドキシンがどのようにスイッチのオンオフを行うのかを解析できるようになると期待される。
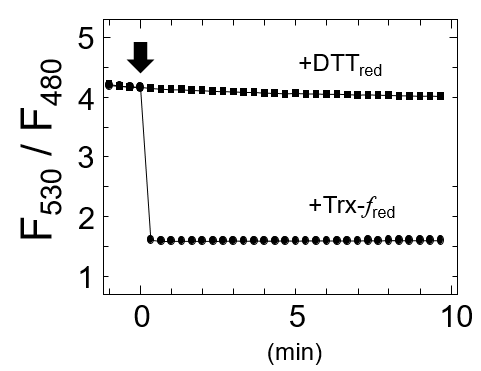
図2. f型チオレドキシンによるCROSTの還元と蛍光強度変化
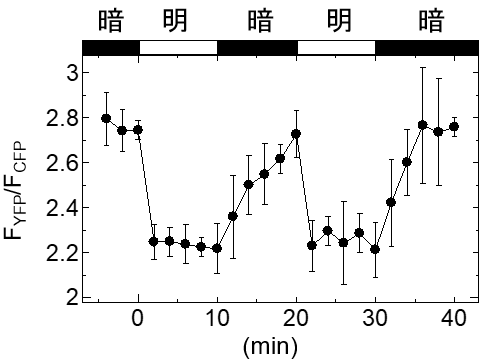
図3. シロイヌナズナ緑葉中のCROSTの明暗条件による蛍光変化
近年の研究により、植物の葉緑体内では様々な代謝系の酵素分子が明暗条件の変化に応答して、還元されたり酸化されたりすることで、その活性を変化させていることがわかってきた。明暗によるタンパク質の状態変化の研究は、単純に光をオンオフすることで達成される明条件と暗条件の比較によって行われているが、自然界での光環境の変動はそれほど単純ではない。
夜明けと日暮れ時には、次第に明るくなる、暗くなるということが起こるし、日中でも木陰では光強度が常に揺らいでいる。このように時々刻々と変化する光条件下で、葉緑体内のタンパク質の酸化還元状態がどのように変化するのかを知ることは、酵素の調節がどのように行われるかを調べるための極めて重要な情報になる。
今後、この新たな蛍光センサーを利用して光環境の変動とタンパク質の酸化還元状態の変動、さらに光合成活性の変動の関連を調べれば、将来、植物を利用した高効率の物質生産の研究などにもつながる知見が得られるものと期待される。
本研究は、科学研究費補助金・新学術領域研究「新光合成」(計画班代表:久堀徹教授)の支援を受けて行われた。
用語説明
[用語1] 酸化還元制御機構 : 生体内の酸化還元状態に応じて、タンパク質分子の持っているジスルフィド結合の形成・開裂などを制御することにより、そのタンパク質の酵素活性を調節する分子機構。タンパク質の翻訳後修飾のひとつ。
[用語2] チオレドキシン(Trx) : ほとんどすべての生物が普遍的に持っている、酸化還元制御に中心的な役割を果たす酸化還元タンパク質。-WCGPC-(-Trp-Cys-Gly-Pro-Cys-)というよく保存された活性部位モチーフを持ち、この2つのCys(システイン)のチオール基の酸化還元によって還元力伝達を行う。
[用語3] 蛍光タンパク質センサーCROST(Change in redox state of thioredoxin) : 本研究で新たに作成したチオレドキシンの酸化還元状態の変化を蛍光変化としてモニターできるようにしたセンサータンパク質。
[用語4] システインのチオール基 : システインというアミノ酸の側鎖。SH基とも呼ばれ、反応性が高くタンパク質の機能に重要な役割を果たすことが多い。
[用語5] ジスルフィド結合 : システインのチオール基同士が酸化条件で形成する共有結合のこと。硫黄原子同士の結合であるため、SS結合とも呼ばれる。
[用語6] YFP/CFP : GFP(緑色蛍光タンパク質)の変異体。YFPは黄色の、CFPはシアン色の蛍光を発する。
論文情報
掲載誌 : |
Journal of Biological Chemistry |
論文タイトル : |
The thioredoxin (Trx) redox-state sensor protein can visualize Trx activities in the light-dark response in chloroplasts |
著者 : |
Sugiura K, Yokochi Y, Fu N, Fukaya Y, Yoshida K, Mihara S, Hisabori T |
DOI : |
お問い合わせ先
東京工業大学 科学技術創成研究院 化学生命科学研究所
教授 久堀徹
E-mail : thisabor@res.titech.ac.jp
Tel : 045-924-5234 / Fax : 045-924-5268
取材申し込み先
東京工業大学 広報・社会連携本部 広報・地域連携部門
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661