東工大ニュース
東工大ニュース
公開日:2019.06.13
東京工業大学 物質理工学院 材料系の福井慧賀大学院生、元素戦略研究センターの飯村壮史助教、細野秀雄栄誉教授の研究グループは、中温域で世界最高のヒドリドイオン伝導度を示す化合物「酸水素化ランタン(LaH3−2xOx)」を発見した。
高伝導度実現の要因はしばしばみられる活性化エネルギーの低下ではなく、これまで大幅な変化に乏しかった前指数因子[用語1]が数桁にわたり増加したことによる。その原因はヒドリドイオンの特徴(小さな質量と大きな分極率)と水素同士の距離が極めて近くに来るという結晶構造に起因することを解明した。
水素の陰イオンであるヒドリドイオンは高い還元電位[用語2]とイオン伝導[用語3]に適した小さなイオン半径と価数を持ち、次世代の電気化学デバイスや化学合成プロセスへの応用が期待されている。化学反応や燃料電池を用いた発電は高い反応効率と反応選択性、高電流密度などの利点を両立できることから中低温域(100-600 ℃)で作動するプロトンやヒドリドイオンの固体電解質が切望されていた。今回創出したLaH3−2xOxはこれを満たすものである。
研究成果は6月12日に英国科学誌「Nature Communications(ネイチャー・コミュニケーションズ)」に掲載された。
水素はさまざまな化成品の原料となるだけでなく、燃料電池の原料として用いることでCO2を排出しないクリーンなエネルギー源にもなる有用な元素である。化学反応を用いるこれらのプロセスでは作動温度を上げるほど反応速度を高めることができる一方で、“効率”(選択率や発電効率)は低温ほど高くなる。そのため、100-600 ℃程度の中温域での運用が適しているとされている。
水素を利用するためにはプロトン(H+)伝導体など「水素を運ぶ材料」が不可欠である。しかし、低温で高いH+伝導度を示す酸水溶液や固体酸は高温では分解してしまい、逆に高温側では塩基である水酸基のプロトンが動き始めるが、低温では全く動かない。これはH+が非常に小さいイオン半径を持つために電荷密度が大きく、容易に陰イオンに束縛されてしまうためである。このH+伝導体における中温-高伝導度の領域は「ノルビーギャップ」と呼ばれ、効率的に水素を使う上で大きな技術障壁となっている(図1)。
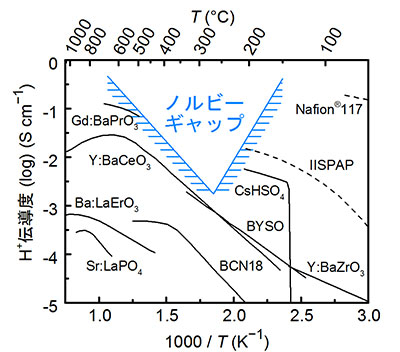
図1. プロトン伝導体におけるノルビーギャップ[参考文献1]
この問題を解決する一つの方法として「ヒドリドイオン(H−)」の利用があげられる。H−は一つの陽子と二つの電子から成る水素の陰イオンである。H−は酸化物イオン(O2−)と同程度のイオン半径を持っておりH+と比べて電荷密度が圧倒的に低い。そのため、H+とは異なる伝導を示し、ノルビーギャップを克服できると考えた。さらにH−の酸化還元電位は−2.3 Vとマグネシウム(−2.36 V)に匹敵するほど還元力が高い。この特徴は水素化還元反応を促進する可能性を秘めており、燃料電池をはじめ多様な化学合成プロセスにおいてメリットが大きい。
新規H−伝導体の候補として酸水素化ランタン(LaH3−2xOx)に着目した。Laは分極率が大きく、H−伝導の活性化エネルギーを低減させることができる。O2−は二つのH−と置換し格子内にH−の空孔を作る。酸素の置換量を変化させることでH−と空孔の量を制御し、高H−伝導を狙った。図2aにLaH3−2xOxの結晶構造を示す。近接した四面体サイト(T-site)と八面体サイト(O-site)の両方にH−が部分的に占有しており、H−の伝導経路を形成する空孔が導入できていることが分かる。酸素量xは0 ≤ x ≤ 1の広い範囲で連続的に制御することができ、その間結晶構造はLaH3と同様に面心立方格子を保つ。
イオン伝導度および電子伝導度はそれぞれ交流インピーダンス法[用語4]、直流分極法[用語5]を用いて評価した。図2bに340 ℃での電子伝導度とイオン伝導度およびイオン輸率[用語6]の酸素量依存性を示す。酸素量(x)の増加に伴って電子伝導度は急激に減少するが、イオン伝導度は0.125 ≤ x ≤ 0.5の範囲で10−2 Scm−1以上の高い値を維持した。その結果、x = 0.25、0.5においてイオン輸率は99%以上となった。また、第一原理分子動力学シミュレーション[用語7]を用いてH−とO2−の伝導を解析したところ、O2−は350 ℃では全く動くことはできず、H−だけが伝導に寄与していることを確認した(図2c)。
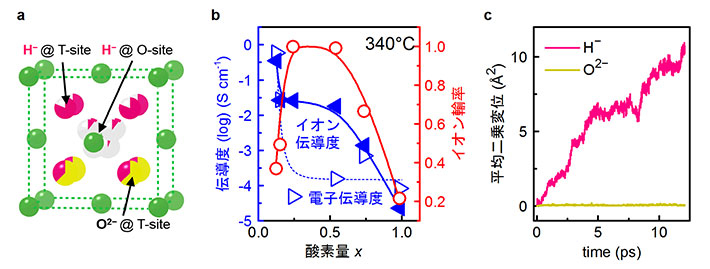
図3aにLaH3−2xOxと既報のヒドリドイオン伝導体のイオン伝導度のアレニウスプロット[用語8]を示す。x = 0.25、0.50におけるLaH3−2xOxのH−伝導度はノルビーギャップを克服し、340 ℃で2.6×10−2 Scm−1とこれまでに世界で報告された中で最も高い値を示した。図3bに活性化エネルギー(Ea)[用語9]とアレニウス式の前指数因子(A)のx依存性を示す。Eaはxに依存せず1.2 eVほどと既報のヒドリドイオン伝導体より2倍程度大きい。一方、Aはxの減少に伴い4桁以上上昇し、通常のイオン伝導体の前指数因子(105-108)と比べ極端に大きい。これは強い非調和性によりEaが温度に依存して変化したためと考えた。
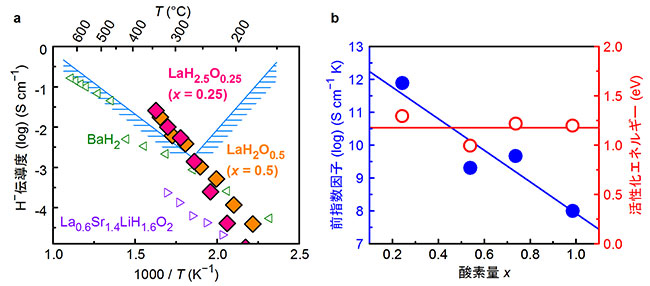
まとめると、この系で世界最高のヒドリドイオン伝導度が得られた要因として以下の3つが挙げられる。1つ目は水素の軽さにある。質量の小さい水素の振動は振幅が大きく非調和性をまといやすい。しかし、これはH+にもH−にも共通した特徴である。2つ目は柔らかいH−イオンが持つ大きな電子分極であり、これは電子を持たず硬いイオンとみなされるH+とはまったく異なる性質である。そして3つ目は、LaH3−2xOx中のH−間距離がLa- H−間距離よりも有意に短いために、H−副格子がより分極しやすいことがあげられる。
今回の結果から、LaH3−2xOxがノルビーギャップを克服する中温域高速H−伝導体として有望であることを示すことができた。今後H−を用いた新たなエネルギーデバイスや化学合成プロセスへの応用が期待される。
用語説明
[用語1] 前指数因子 : イオン伝導度の温度依存性を表すアレニウスの式(σT = Aexp(−Ea/RT))の指数の前に現れる温度に依存しない定数項。イオンの振動数、ホッピング距離、イオンの濃度などの物理量から構成される。
[用語2] (酸化)還元電位 : 電子のやり取りの際に発生する電位。電子の放出しやすさ、あるいは受け取りやすさを定量的に評価する尺度となる。
[用語3] イオン伝導 : 電場下でイオンが伝導すること。金属の電気伝導は主に電子の伝導が支配的だが、イオン伝導体では、イオンの伝導が支配的になる。
[用語4] 交流インピーダンス法 : 電極間に交流を印加し、交流の周波数を変化させた時のインピーダンスを測定することでイオン伝導率や誘電率、化学反応の追跡などを行う測定手法。
[用語5] 直流分極法 : 試料の電極に電圧を印加し、電流値と印加電圧から伝導度を測定する手法。片方の電極には主たる伝導種であるイオンを透過しない電極を用い、イオンの流れ止めることでその他の伝導種に起因する電流を測定する。
[用語6] イオン輸率 : 全伝導度(電子伝導度とイオン伝導度)に対するイオン伝導の割合。
[用語7] (第一原理)分子動力学シミュレーション : 原子ならびに分子の物理的な動きの時間発展を計算するコンピューターシミュレーション手法。原子や分子、電子の相互作用を第一原理計算から求める手法を特に第一原理分子動力学シミュレーションと呼ぶ。
[用語8] アレニウスプロット : 縦軸にσTの対数(ln(σT))、横軸に温度の逆数1/Tをとりアレニウスの式(σT = Aexp(−Ea/RT))をプロットしたもの。この時、傾きは−Ea/R、切片はlnAになる。σ、A、Ea、Rは、イオン伝導度、前指数因子、活性化エネルギー、気体定数。
[用語9] 活性化エネルギー : イオンが拡散する際に飛び越えなければならないエネルギー障壁。
論文情報
掲載誌 : |
Nature Communications |
論文タイトル : |
Characteristic Fast H− Ion Conduction in Oxygen-Substituted Lanthanum Hydride(酸素置換水素化ランタンにおける特徴的な高速ヒドリドイオン伝導) |
著者 : |
Keiga Fukui, Soshi Iimura, Tomofumi Tada, Satoru Fujitsu, Masato Sasase, Hiromu Tamatsukuri, Takashi Honda, Kazutaka Ikeda, Toshiya Otomo, Hideo Hosono(福井慧賀、飯村壮史、多田朋史、藤津悟、笹瀬雅人、玉造博夢、本田孝志、池田一貴、大友季哉、細野秀雄) |
DOI : |
参考文献
[1] T. Norby; Solid-state protonic conductors: principles, properties, progress and prospects; Solid State Ion., 125, 1 (1999).
[2] M. C. Verbraeken, C. Cheung, E. Suard, and J. T. S. Irvine; High H− ionic conductivity in barium hydride; Nat. Mater. 14, 95 (2015).
[3] G. Kobayashi, Y. Hinuma, S. Matsuoka, A. Watanabe, M. Iqbal, M. Hirayama, M. Yonemura, T. Kamiyama, I. Tanaka, R. Kanno; Pure H– conduction in oxyhydrides; Science 351, 1314 (2016).
お問い合わせ先
東京工業大学 元素戦略研究センター
助教 飯村壮史
E-mail : s_iimura@mces.titech.ac.jp
Tel : 045-924-5197
東京工業大学 元素戦略研究センター
栄誉教授 細野秀雄
E-mail : hosono@mces.titech.ac.jp
Tel : 045-924-5009
取材申し込み先
東京工業大学 広報・社会連携本部 広報・地域連携部門
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661