東工大ニュース
東工大ニュース
公開日:2022.07.26
東京工業大学 生命理工学院 生命理工学系のErinn Sim Zixuan大学院生(研究当時)、榎本孝幸研究員、白木伸明准教授、粂昭苑教授、京都大学大学院生命科学研究科の神戸大朋准教授らの研究グループは、東京大学、熊本大学、味の素株式会社などと共同で、ヒト多能性幹細胞(pluripotent stem cells:PSC)[用語1]の未分化性維持にメチオニン代謝[用語2]と亜鉛[用語3]が寄与することを明らかにし、それぞれの除去培地を組み合わせて利用する新たな膵臓β細胞への分化誘導方法を開発した。
ヒト多能性幹細胞からの膵臓β細胞の分化誘導では、細胞株ごとに分化誘導効率が異なるという問題がある。本研究グループはこれまでの研究で、多能性幹細胞の未分化性の維持や分化誘導に、メチオニンやその代謝物が重要であることを明らかにしてきた。
本研究では、幹細胞の分化制御におけるメチオニン代謝の下流シグナルを明らかにするため、網羅的遺伝子発現解析を行った。その結果、メチオニン欠乏によって亜鉛排出トランスポーターSLC30A1[用語4]が有意に増加した。そこで細胞内亜鉛濃度を測定した結果、5時間のメチオニン欠乏で幹細胞内のタンパク質結合型亜鉛が有意に減少した。この亜鉛濃度低下には、メチオニン代謝物であるホモシステインが寄与することもわかった。次に、味の素株式会社と共同で新たに開発した亜鉛除去培地で幹細胞を数日間培養して、亜鉛含量低下を再現したところ、メチオニン欠乏によって引き起こされる現象の一部(増殖抑制・メチオニン代謝変動・分化状態移行)を模倣することを確認した。これらの結果から、メチオニン欠乏は、幹細胞内の亜鉛含有量を低下させることにより、細胞分化を促すと結論づけた。
さらに、開発した亜鉛除去培地を用いて、複数の多能性幹細胞を効率的に内胚葉へ分化させることに成功した。最終的にはメチオニン欠乏と亜鉛欠乏を組み合わせることで、多能性幹細胞から機能的な膵臓β細胞を分化誘導する新規培養方法を確立した。
本研究成果は、多能性幹細胞の未分化性維持や分化におけるアミノ酸とミネラルの関連性を世界で初めて明らかにし、培養液中の栄養因子が細胞分化に重要な役割を果たすことを示すものである。今後、これらの栄養因子が細胞分化に与える影響を詳細に把握することは、再生医療や創薬研究に利用可能な細胞製造に有益である。
研究成果は「Cell Reports」に7月19日(現地時間)に掲載された。
膵臓β細胞はインスリンを分泌し、血中グルコース濃度の維持に寄与している。1型糖尿病は膵臓β細胞が破壊された結果、インスリンがほとんどまたはまったく分泌されないことで起こる病気であり、根治療法としては膵臓及び膵島移植があるが、ドナーは圧倒的に不足している。そこで、新たな移植源として、ヒト多能性幹細胞の利用が試みられている。これまでに粂教授・白木准教授らの研究グループも含め、多くの研究者が膵臓β細胞の分化誘導法開発を行ってきたが、細胞株ごとに分化誘導効率が異なることが問題であった。
幹細胞から目的の細胞を分化させるためには、最適な細胞分化培養液が必要であり、この培養液はアミノ酸・糖・ビタミン・ミネラルなどの栄養素を含む基礎培地と、成長因子およびシグナル阻害薬から構成される。本研究グループは、基礎培地に注目した分化誘導方法開発を行ってきた。これまでに、多能性幹細胞は未分化性を維持するためにメチオニンの代謝物であるS-アデノシルメチオニン(SAM)[用語5]を必要とし、メチオニン欠乏は幹細胞内のSAM減少を引き起こして、分化に適した状態に移行させることを報告している。さらにメチオニンを除去した幹細胞培地を開発し、初期分化促進および分化時に残存する未分化細胞の選択的除去に成功しており、これによって細胞株によらず効率的に内胚葉を分化誘導することが容易になった(白木ら、Cell Metab., 2014)。
本研究では、膵臓分化を開始する直前5時間のメチオニン欠乏がその後の内胚葉・膵臓前駆細胞・膵臓β細胞への分化を顕著に促進することを確認したうえで、このメチオニン欠乏による分化促進機構の解明に取り組んだ。
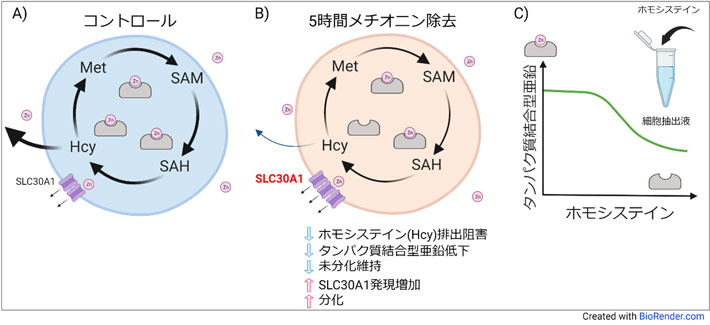
メチオニン代謝の下流シグナルを明らかにする目的で網羅的遺伝子発現解析を行った結果、メチオニン欠乏により多能性幹細胞において亜鉛排出トランスポーターSLC30A1遺伝子が有意に増加することを見出した。そこで、化学形態別亜鉛濃度測定法[用語6]を用いて亜鉛濃度を測定したところ、メチオニン除去培地で5時間培養した場合に、幹細胞内のタンパク質結合型亜鉛が有意に減少することがわかった(図1A、B)。このSLC30A1発現増加や亜鉛含量低下は、他の必須アミノ酸除去と比較してメチオニン除去で顕著であった。また未分化多能性幹細胞に特異的な現象で、多能性幹細胞由来内胚葉やがん細胞株では確認できなかった。
次に、通常時にはメチオニン代謝物であるホモシステインが細胞外へ積極的に排出されるが、メチオニン欠乏時はその排出が顕著に抑制される点と、ホモシステインがスルフヒドリル基(SH基)を持ち、亜鉛と結合するタンパク質から亜鉛を追い出すことが可能である点に着目して、細胞抽出液を用いたホモシステイン添加実験を行った。その結果、添加したホモシステイン濃度に依存してタンパク結合型亜鉛濃度が低下した(図1C)。この結果から、メチオニン欠乏はホモシステインを介して、幹細胞内のタンパク質結合型亜鉛を減少させることが明らかになった。
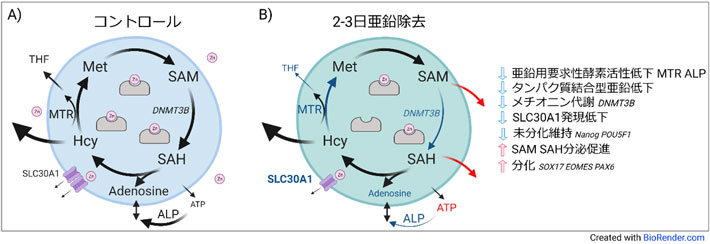
次に、細胞内亜鉛含量の操作を目的として亜鉛を除去した幹細胞培地を、味の素株式会社と共同で新たに開発した。この培地でヒト多能性幹細胞を数日間培養することで、亜鉛含量低下を再現したところ、MTRやALPといった亜鉛要求性酵素の活性低下が見られ、メチオニン欠乏によって引き起こされる現象の一部(増殖抑制・メチオニン代謝変動・分化状態移行)を模倣することを確認した(図2)。以上のことから、メチオニンは、細胞内亜鉛濃度を制御することで多能性幹細胞の未分化状態を維持していると結論づけた。
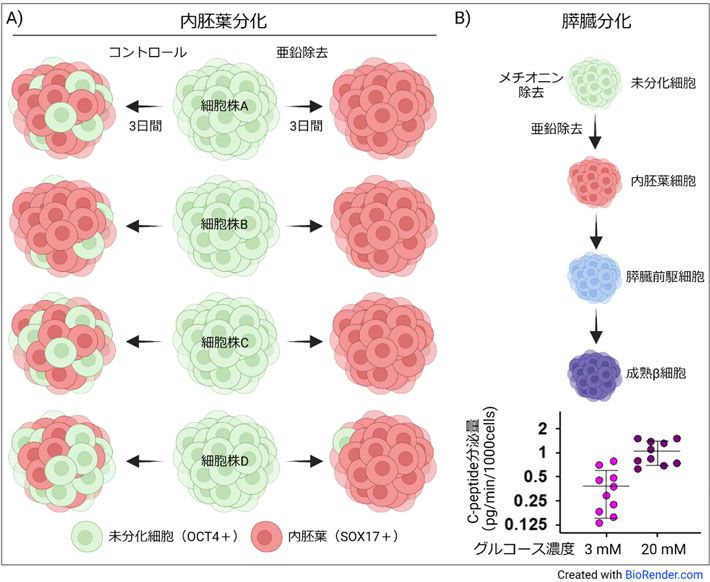
次に、未分化維持状態における亜鉛欠乏が幹細胞を分化傾向に変化させることを踏まえて、内胚葉分化時に亜鉛除去が与える影響を複数の細胞株で評価した。亜鉛を含むコントロール条件では、細胞株ごとに内胚葉分化効率が異なるが、亜鉛除去培地を内胚葉分化に利用することでどの細胞株でも効率的にSOX17陽性の内胚葉細胞へ分化できるようになった(図3A)。さらに、未分化時のメチオニン欠乏と内胚葉分化時の亜鉛欠乏を組み合わせることで、ヒト多能性幹細胞から効率的に膵臓細胞を分化させ、最終的に糖応答性インスリン分泌能[用語7]を持つ成熟膵臓β細胞への分化誘導に成功した(図3B)。
本研究で開発した多能性幹細胞から膵臓β細胞への分化誘導方法では、未分化細胞の混入を抑制し、造腫瘍性リスクを回避できる。またどんな細胞株にも応用でき、膵臓以外の臓器への分化誘導にも応用できることから、汎用性の高い分化誘導方法だといえる。
今後は、本研究で開発した新規分化誘導方法を用いて、成熟膵臓β細胞を用いた再生医療研究を推進したい。また、幹細胞から目的の細胞を分化させるためには、本研究で注目したメチオニンや亜鉛などの栄養素を含む基礎培地に加えて、成長因子・シグナル阻害薬から構成される分化培養液が必要であり、その開発も進めていく予定である。本研究で取った基礎培地の栄養組成至適化による分化制御という戦略は、膵臓以外の臓器への分化誘導にも応用可能であり、今後の再生医療や創薬研究に利用可能な細胞製造に有用である。
付記
本研究は、東京工業大学生命理工学院のErinn Sim Zixuan大学院生(研究当時)、榎本孝幸研究員、古田奈央大学院生(研究当時)、小澤弘樹大学院生、白木伸明准教授、粂昭苑教授、東京大学大学院薬学系研究科の樫尾宗志朗助教、三浦正幸 教授、京都大学大学院生命科学研究科の神戸大朋准教授、熊本大学生命科学研究部の津山友徳特任助教、味の素株式会社の荒川哲大研究員、横山水穂研究員からなる研究チームによって行われた。
用語説明
[用語1] 多能性幹細胞(pluripotent stem cells:PSC) : 自己複製能と多分化能を併せ持ち、体を構成するほぼすべての細胞に分化できる幹細胞であり、胚性幹細胞(embryonic stem cells : ESCs)と人工多能性幹細胞(induced pluripotent stem cells : iPSCs)が含まれる。
[用語2] メチオニン代謝 : メチオニン代謝は葉酸代謝や、コリン・ベタインの代謝系と共役するため、DNAやヒストンメチル化に影響を与える。メチオニン・Sアデノシルメチオニン・Sアデノシルホモシステイン・ホモシステインからなるメチオニン代謝回路を形成している。
[用語3] 亜鉛 : 必須微量元素である亜鉛は、生体内でタンパク質構造安定化因子、酵素活性化因子、シグナル因子などとして幅広い役割を担う。ヒトゲノムにコードされている全タンパク質の10%程度が亜鉛結合モチーフを持つ。亜鉛には様々なタンパク質の立体構造を安定させる役割(例:Zinc finger転写因子、インスリンの安定化)や、300種類以上の亜鉛要求性酵素を活性化する役割(例:DNA/RNAポリメラーゼ、メチオニンシンターゼMTR、アルカリフォスファターゼALP)がある。細胞にとって、亜鉛恒常性維持は生存に直結する最重要事項の一つである。
[用語4] 亜鉛排出トランスポーターSLC30A1 : 亜鉛トランスポーターZnT1をコードする遺伝子であり,細胞質膜表面に局在する唯一のZnTファミリー分子である。細胞内の亜鉛を細胞外に輸送する経路において重要な役割を果たす。
[用語5] S-アデノシルメチオニン(SAM) : メチオニン代謝物の中間代謝物であり、生体内の様々なメチル化反応においてメチル基供与体として働く。
[用語6] 化学形態別亜鉛濃度測定法 : HPLC-ICP-MSという高速液体クロマトグラフィー (HPLC; High performance liquid chromatography)と、誘導結合プラズマ質量分析計(ICP-MS; Inductively Coupled Plasma-Mass Spectrometer)とを組み合わせた測定機器を用いた、化学形態別の亜鉛濃度測定法。タンパク質に結合した亜鉛と遊離型の亜鉛を区別して測定することが可能。
[用語7] 糖応答性インスリン分泌能 : 外環境のグルコースに応じて、細胞からインスリンを分泌する能力。評価としては、インスリン生合成時にできる副産物であり、インスリンと同程度の割合で分泌されるC-ペプチドがインスリン分泌の指標となっている。
論文情報
掲載誌 : |
Cell Reports |
論文タイトル : |
Methionine metabolism regulates pluripotent stem cell pluripotency and differentiation through zinc mobilization |
著者 : |
Erinn Zixuan Sim, Takayuki Enomoto, Nobuaki Shiraki, Nao Furuta, Soshiro Kashio, Taiho Kambe, Tomonori Tsuyama, Akihiro Arakawa, Hiroki Ozawa, Mizuho Yokoyama, Masayuki Miura, Shoen Kume |
DOI : |
お問い合わせ先
東京工業大学 生命理工学院 生命理工学系
教授 粂昭苑
Email skume@bio.titech.ac.jp
Tel 045-924-5812 / Fax 045-924-5813
東京工業大学 生命理工学院 生命理工学系
准教授 白木伸明
Email shiraki@bio.titech.ac.jp
Tel 045-924-5814 / Fax 045-924-5813
取材申し込み先
東京工業大学 総務部 広報課
Email media@jim.titech.ac.jp
Tel 03-5734-2975 / Fax 03-5734-3661
京都大学 総務部広報課国際広報室
Email comms@mail2.adm.kyoto-u.ac.jp
Tel 075-753-5729