東工大ニュース
東工大ニュース
公開日:2022.09.13
東京工業大学 科学技術創成研究院 化学生命科学研究所の上田宏教授と同大学 生命理工学院 生命理工学系のDai Yancen(ダイ・ヤンセン)大学院生、科学技術創成研究院 細胞制御工学研究センターの佐藤優子助教と木村宏教授、シンガポール科学技術研究庁のF.A. Ghadessy(ファリッド・ガデシー)主席研究員らは、細胞内抗原に結合すると光る抗体断片Intra Q-bodyを細胞内に導入することにより、生細胞内タンパク質存在量の時空間的変化を観察できるバイオセンサー[用語1]として用いることに成功した。
これまで研究グループでは、蛍光色素で部位特異的に化学修飾[用語2]した抗体断片であるクエンチ抗体(Quench body/Q-body)[用語3]を構築してきた。Q-bodyは、励起光を照射したときの蛍光強度の変化を見ることで、抗原としてさまざまな物質を検出できる。しかしこれまでは、細胞表面にあるバイオマーカータンパク質の簡便な検出は可能だったが、細胞内タンパク質の検出やイメージングには成功していなかった。
今回研究グループでは、がん抑制タンパク質であるp53を細胞内で高い応答で検出できる、安定なQ-Body(Intra Q-body)を構築した。これを細胞内に電気穿孔法[用語4]を利用して導入することで、固定化細胞のみならず、洗浄が不可能な生細胞内でもガン抑制タンパク質p53[用語5]のリアルタイムイメージングに成功した。
このIntra Q-bodyを用いたシステムでは、抗がん剤投与による生細胞内でのp53量の時間変化を、高い応答と精度で24時間以上にわたり観察できた。さらに、発現量の異なる細胞群の中からp53発現細胞のみをセルソーターで濃縮することにも成功した。
この方法によれば、今後さまざまな細胞内バイオマーカー発現細胞を簡便に検出・単離でき、将来的には効果的な細胞治療につながると期待される。
この成果は、英国時間8月1日に英国化学誌「Chemical Science(ケミカル・サイエンス)」にオンライン掲載された。
抗原抗体反応[用語6]を活用してさまざまな物質の存在や濃度を診断する免疫測定法は、生物学の基礎研究、臨床診断、食品安全管理、環境保全などの幅広い分野で不可欠な測定法となっている。この免疫測定法に活用可能なセンサータンパク質として、上田研究室で研究を継続してきたクエンチ抗体(Q-body)は、抗原結合部位を持つ抗体断片の一部に、蛍光色素によって化学修飾を行ったものである。
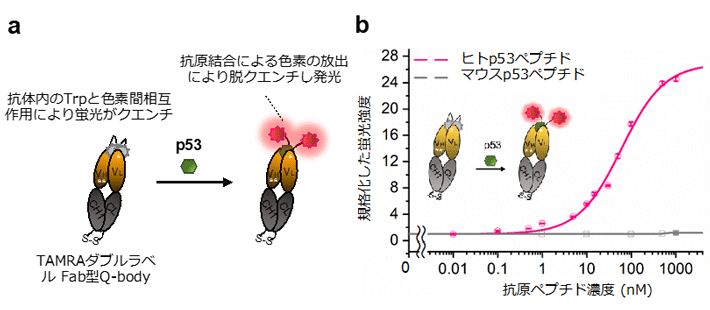
Q-bodyに付加した蛍光色素は、抗原となる物質が存在しない状態では、主に抗体内のアミノ酸の一種であるトリプトファン(Trp)残基からの光誘起電子移動[用語7]あるいは色素間相互作用[用語8]によって消光(クエンチ)されている。しかし抗原を加えると、抗原との結合により蛍光色素が抗体分子から放出されて消光が解消し、蛍光が回復する。そのためQ-bodyは、蛍光強度のみを測定することで、抗原となる物質を簡便かつ迅速に検出できる測定素子として、さまざまな分析への応用が行われてきた。例えばこれまでに、Q-bodyを用いることで、細胞表面のがんマーカータンパク質であるHER2[用語9]やクローディンなどを、結合反応後の洗浄操作が必要な蛍光標識抗体を用いる場合よりも簡便に検出することに成功している。
ただしこのような細胞表面ではなく、細胞内のタンパク質を対象とした抗体による蛍光検出では、いくつかの技術的ハードルがあった。第一に、細胞を有機溶媒などで固定化すれば、膜に開いた穴から蛍光標識抗体を導入して染色する従来の免疫蛍光法を使用できるが、その操作で細胞は死んでしまうため、生細胞内での検出はできなかった。第二に、何らかの方法で生細胞内に蛍光標識抗体を導入できても、ターゲット抗原に結合しない抗体も蛍光を発してしまうため、これが高いバックグラウンドとなってターゲット抗原の明瞭な蛍光観察が難しかった。これら以外の方法として、細胞内で安定に発現可能な抗体(Intrabody)[用語10]と蛍光タンパク質の融合タンパク質をコードする遺伝子を細胞に導入し、抗体の発現量を調節することで、細胞内抗原の局在を観察することも可能だが、Intrabodyの取得と、遺伝子操作した後の細胞の利用が難しい問題があった。
そこで本研究では、細胞内抗原に対する抗体を用いて安定なQ-bodyを構築し、これを比較的高い効率で均一に細胞に導入可能な電気穿孔法を用いて生細胞内に導入することで、これらの問題を克服することを目指した。
本研究では、蛍光色素としてTAMRAという有機色素を選択するとともに、がん抑制タンパク質であり、がん診断マーカーでもあるp53を検出対象として用いることで、細胞内抗原に結合すると光るQ-body(「Intra Q-body」)の構築を行った。
今回Q-body化を試みたp53抗体DO-1は、基礎研究や診断で汎用される優れた抗体である一方で、Q-body化するために大腸菌発現系を用いて組換え抗体を調製した場合、抗体の発現量が少なすぎる問題があった。そこで、他の抗体では出現頻度の低いアミノ酸残基をより頻度が高いものに置換した一本鎖抗体scFvライブラリを構築し、高い信号を示すクローンを選択したところ、分泌発現効率が顕著に向上した変異体C11が得られた。
そこでこのクローンC11を用いていくつかの形状のQ-bodyの応答を検討したところ、scFvをFabに変換し、そのH鎖とL鎖の両方のアミノ末端をTAMRAで修飾したQ-body(Fab型Q-body)において、緩衝液中でnM以下の濃度から、最大27倍という高い抗原p53ペプチド依存的な蛍光応答を得ることに成功した(図1)。
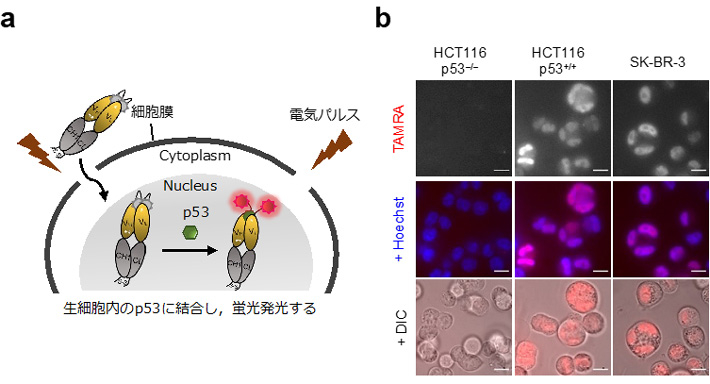
こうして構築されたIntra Q-body(Fab型Q-body)を用いて、固定化・透過処理したヒト結腸がん細胞株HCT116(+/+)を染色(洗浄操作はせず)したところ、従来型のTAMRA標識抗体に比べて顕著に高い、p53ノックアウト細胞HCT116(–/–)の8.3倍の蛍光が見られ、バックグラウンド蛍光が低減可能なIntra Q-bodyの優秀さが示された。
次にこの結果を踏まえて、生細胞中のp53のイメージングを試みた。p53 Intra Q-bodyを電気穿孔法によって、p53を発現しない細胞株HCT116(–/–)p53と、3種類のp53発現がん細胞(HCT116(+/+)およびSK-BR-3)に導入したところ、p53発現がん細胞の核内で顕著なTAMRA由来の蛍光が観察された(図2)。
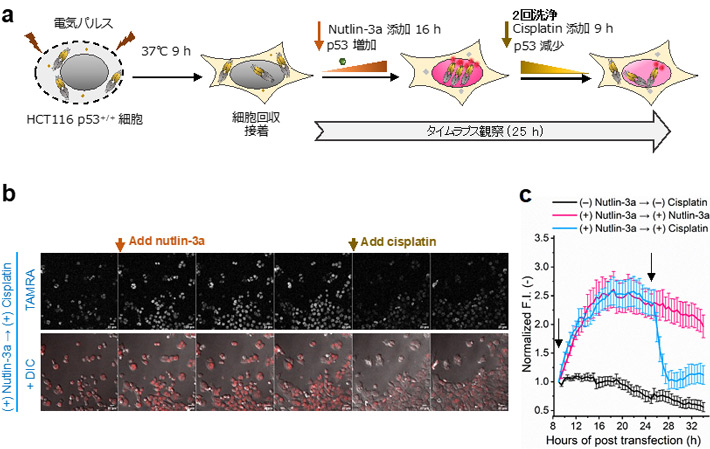
次に、Intra Q-bodyを導入したHCT116(+/+)細胞を長期間培養し、細胞内のp53濃度変化がどの程度追跡できるか、ライブイメージング法により検討した。Intra Q-body導入後、時間をおいて細胞を2種類の抗がん剤(Nutlin-3aとCisplatin)で処理することで、細胞内のp53を蛍光シグナルとして経時観察した。その結果、Intra Q-bodyが導入されたほぼ全ての細胞において、p53の分解因子であるMdm2の阻害剤Nutlin-3aはp53量を増加させたが、DNA合成阻害剤であるCisplatinはp53量を低下させることが、蛍光イメージングとウエスタンブロッティングの両者で確認された。この結果から、今回構築したIntra Q-bodyを用いて、生細胞中のp53量の時空間変化を観察できることが確かめられた(図3)。
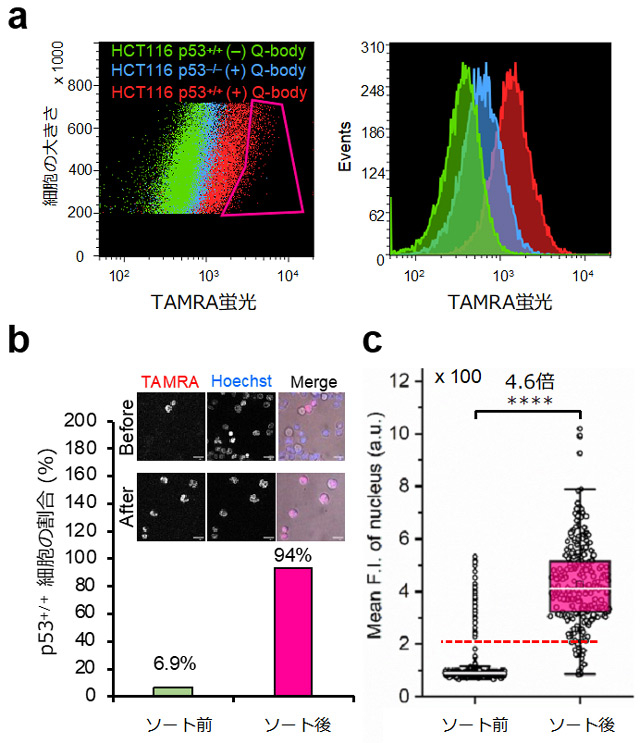
最後に、この方法で生細胞内抗原量が測定できることを利用し、通常は細胞膜上の抗原を用いなければ生細胞を分取できないセルソーターを用いて、細胞をp53発現の有無で分離することを試みた。p53を発現しないHCT116(–/–)細胞と、p53を発現するHCT116(+/+)細胞を混合し、蛍光陽性細胞群を分取したところ、94%の細胞がHCT116(+/+)細胞であったことから、本手法が細胞内抗原を用いた細胞分取に応用できることが示された(図4)。
この研究により、Intra Q-body化した抗体を用いることで、これまで観察できなかった生きた細胞内タンパク質の量と局在を高い画質で可視化でき、さらに細胞を高精度で「ふるい分け」できることが示された。この方法によれば、p53が過剰発現しているがん細胞や、ウイルスに感染した細胞を集めて解析したり、制御性T細胞におけるFoxP3などの特定の転写因子を発現している細胞を集めて治療に用いたりすることが可能となり、基礎研究に貢献できるだけでなく、診断医療の進歩に寄与することが期待される。
今回研究チームは、高性能なp53 Intra Q-bodyを開発し、蛍光標識抗体をこれまで困難だった生細胞内で機能させることに成功した。Intra Q-bodyは、消光されている蛍光色素が抗原との結合によって蛍光回復するという、従来の蛍光標識抗体とは異なる新しい検出原理に基づいており、今後同様の方法を用いて、多くの細胞内抗原検出系を創出できる可能性がある。また、今回はIntra Q-bodyを細胞内に導入する際に、技術的に確立された電気穿孔法を用いたが、今後は近年報告の増えているペプチド系試薬などを用いることで、より多くの人がIntra Q-bodyを試せるようにしたいと考えている。
付記
本研究は、科学研究費助成事業 基盤研究(A)、科学技術振興機構(JST)未来社会創造事業、国際科学技術共同研究推進事業(戦略的国際共同研究プログラム、SICORP)その他の補助を受けて行われた。
用語説明
[用語1] バイオセンサー : 生体分子が持っている機能を、化学物質の存在や濃度を測定するために活用する化学センサー。
[用語2] 化学修飾 : 生体高分子に含まれる、化合物の特性を決める特定原子団の性質を化学的に変化させ、反応などの機能を変化させること。
[用語3] クエンチ抗体 : (Quenchbody/Q-body):抗体の断片を、部位特異的に蛍光色素で化学修飾した抗体。蛍光色素が抗体内のアミノ酸により消光(Quench)される現象を利用して、蛍光強度の変化によって抗原を検出できる。
[用語4] 電気穿孔法 : 細胞に高圧電気パルスをかけ、一時的に膜を破壊し細胞内に核酸やタンパク質などの生体高分子を導入する手法。
[用語5] p53 : がん抑制タンパク質として知られるが、がん細胞では変異したp53が過剰発現することが多く、がん診断マーカーとしても用いられる。なお今回用いたDO-1抗体は、p53上で変異しにくいアミノ酸配列を認識する。
[用語6] 抗原抗体反応 : 抗原と、その特定の抗原に対応する抗体が結合して起こるさまざまな現象。免疫反応やアレルギー反応、アナフィラキシー反応などがあたる。
[用語7] 光誘起電子移動 : 光吸収によって励起状態となった蛍光団と、その近傍に存在する原子団(この場合Trp)との間に生じる電子移動。励起された電子は元の軌道に戻れず、蛍光団由来の蛍光がみられなくなる。
[用語8] 色素間相互作用 : ローダミン類などで複数の色素が近接すると、H-dimerと呼ばれる2量体構造を形成し、その蛍光がクエンチする現象。
[用語9] HER2 : 上皮細胞成長因子受容体2。乳がんや肺小細胞がんなどで高発現し、増殖信号を発する。悪性がんマーカーとして診断と治療に用いられる。
[用語10] Intrabody : 細胞内抗体。細胞内は細胞外に比べて還元的な状態にあるため、構造形成にジスルフィド結合の形成を必要とする通常の抗体は発現しにくいことが知られている。Intra Q-bodyの構築では発現と構造形成を細胞外で行うことで、この問題を回避した。
論文情報
掲載誌 : |
Chemical Science 13, 9739-9748 (2022) |
論文タイトル : |
Intra Q-body: an antibody-based fluorogenic probe for intracellular proteins that allows live cell imaging and sorting |
著者 : |
Yancen Dai, Yuko Sato, Bo Zhu, Tetsuya Kitaguchi, Hiroshi Kimura, Farid J. Ghadessy and Hiroshi Ueda* |
DOI : |
お問い合わせ先
東京工業大学 科学技術創成研究院 化学生命科学研究所
教授 上田宏
Email ueda@res.titech.ac.jp
Tel / Fax 045-924-5248
取材申し込み先
東京工業大学 総務部 広報課
Email media@jim.titech.ac.jp
Tel 03-5734-2975 / Fax 03-5734-3661