東工大ニュース
東工大ニュース
公開日:2022.12.15
東京工業大学 科学技術創成研究院 化学生命科学研究所の朱博助教と上田宏教授、東京医科歯科大学 大学院医歯学総合研究科 生体集中管理学分野の野坂宜之講師と若林健二教授、同医療イノベーション推進センター長の小池竜司教授、中国康復大学の董金華教授らは、抗原に結合すると光る抗体断片Q-body(Quench body、クエンチ抗体)[用語1]を、短時間でコロナウイルス量を検出できるバイオセンサー[用語2]として用いることに成功した。
これまで研究グループでは、抗体断片[用語3]に蛍光色素を化学修飾[用語4]したクエンチ抗体(Q-body)を構築してきた。Q-bodyは、励起光を照射したときの蛍光強度の変化を見ることで、ウイルスを構成する物質の有無や量を検出できる。
今回研究グループでは、まず新型コロナウイルスの構成成分のうちスパイク(S1)タンパク質を検出するQ-bodyを開発し、疑似ウイルス粒子の高感度検出に成功した。さらに、ヌクレオカプシド(N)タンパク質の検出においては、反応条件を最適化することで、東京医科歯科大学病院で採取した臨床サンプル中にある新型コロナウイルス検出ならびに感染有無を判定することに成功した。
また、反応液にポリエチレングリコールなどの高分子を適量添加することで、反応を加速し高感度化できることを明らかにした。
この方法を発展させれば、唾液や鼻咽喉ぬぐい液などから目的病原体を簡便迅速に定量検出でき、将来効果的な診断法につながると期待される。
これらの成果は、英国時間9月15日に科学誌「Scientific Reports(サイエンティフィックレポーツ)」、9月30日に英国化学誌「Analyst(アナリスト)」にオンライン掲載され、特に後者はHot Article(注目論文)と掲載号のBack Cover(裏表紙)に選ばれた。
抗原抗体反応[用語5]を活用してさまざまな物質の存在や濃度を判断する免疫測定法は、生物学の基礎研究、臨床診断、食品安全管理、環境保全などの幅広い分野で不可欠な測定法となっている。この免疫測定法において活用可能なセンサータンパク質として、上田研究室ではクエンチ抗体(Q-body)に関する研究を継続してきた。Q-bodyは、抗原結合部位を持つ抗体断片の一部に、蛍光色素を化学修飾したものである。
Q-bodyに結合している蛍光色素は、抗原となる物質が存在しない状態では、発光しない(消光:クエンチ)状態にある。これは、主に抗体内のアミノ酸残基からの光誘起電子移動[用語6]あるいは色素間相互作用[用語7]の作用によるものである。そこに抗原を加えると、抗原が抗体断片と結合し、それに伴い蛍光色素が抗体分子から脱離・放出される。それによって、蛍光色素が蛍光を呈するようになる。その蛍光強度を測定することで、さまざまな抗原の存在と濃度の判別が可能になる。例えばこれまでに、Q-bodyを用いることで、インフルエンザウイルスのHAタンパク質[用語8]やアミロイドβタンパク質などを、簡便に検出することに成功している。
本研究では、新型コロナウイルス抗原に対する抗体を用いて高感度なQ-bodyを構築した。そしてこれらをセンサーとして用いることで、現在最低15分程度かかる通常の抗原検査よりも迅速な抗原検査を開発し、より簡便な感染の判定に利用することを目指した。
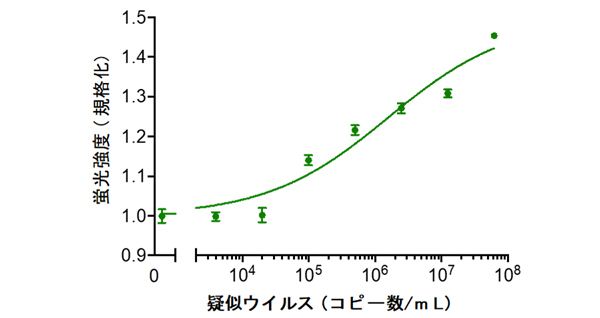
本研究では、まずパンデミックの初期で抗体入手が困難だった時期に、ヒト型抗体提示ファージライブラリ[用語9]から、ウイルス表面にあり感染に重要な役割を果たすS1タンパク質に対して強く結合(Kd値~3 nM)するヒト型組み換え抗体A7を取得した。A7から抗体断片Fabを構築し、その2箇所のN末端をATTO520という蛍光色素で修飾してQ-bodyを構築したところ、疑似ウイルス粒子と混合してから2分後に、1 mLあたり105コピーという低濃度から蛍光検出することに成功した(図2)。しかしながら、S1タンパクを標的とした検出は、ウイルスの株変異にうまく対応できない場合もある問題にも直面した。
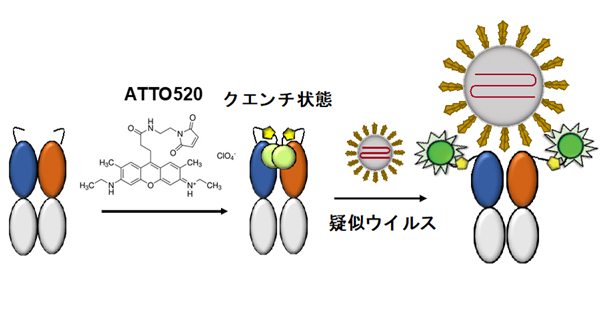
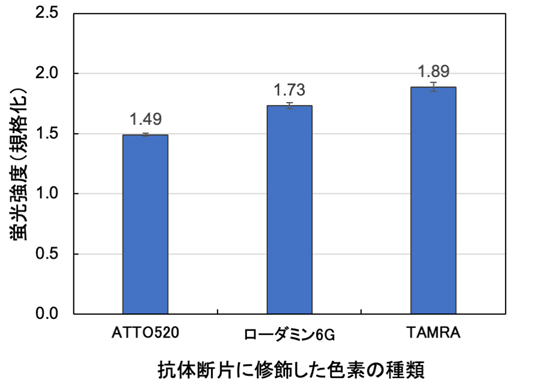
そこで次に、変異体ウイルスにおいても変異が入ることが少なく、患者サンプル中にはSタンパク質より多く含まれるとされるRNA結合(N)タンパク質に対するQ-bodyの構築を試みた。2021年5月に公開されたnCoV396という抗体(Kd~1.0 nM)の構造を元に、A7と同様にFab型Q-bodyを数種類の蛍光色素を用いて構築した所、TAMRAと呼ばれる蛍光色素を修飾したQ-bodyが最も高い蛍光応答を示した(図3)。しかし本抗体は結合反応がやや遅く、A7由来Q-bodyより長めの検出時間を要した。
一般に、溶液中で抗原抗体反応などのタンパク質間相互作用をさせる場合、溶液に適した高分子を加えることで両タンパク質の水中における有効濃度を向上させ、反応速度を加速可能なことが知られている。そこで今回、Q-bodyにいくつかの高分子を加えて検討した結果、平均分子量6,000のポリエチレングリコール(PEG6000)を5%加えることで、反応を有意に加速させることに成功した(図4)。
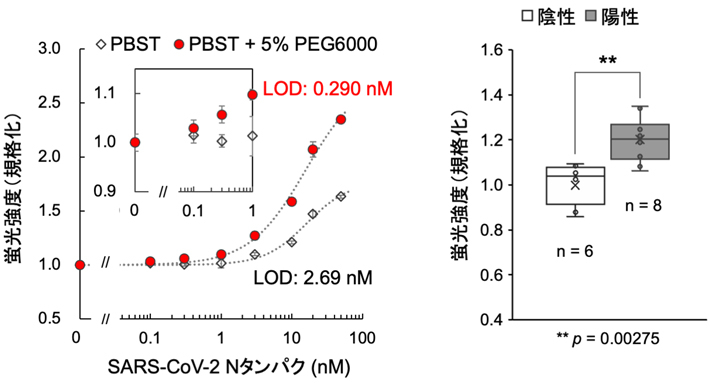
今回構築されたNタンパク質検出用Fab型Q-bodyを用いて、0.3 nM以下の新型コロナウイルスNタンパク質の5分程度での検出が示された。また、ポータブル蛍光測定装置を用いて臨床サンプルの測定に成功した。実現された検出感度は通常のイムノクロマト法による抗原検査キットとほぼ同等だが、検査に必要な手技と通常15分以上とされる反応時間が少ないことから、測定の定量性と再現性はより高いと考えられる。
今回研究チームは、2つのタイプのSARS-CoV-2 Q-bodyを開発し、うち1つを新型コロナ感染症の迅速診断薬として機能させることに成功した。Q-bodyは、消光されている蛍光色素が抗原との結合によって蛍光回復するという、他とは異なる検出原理に基づいており、今後同様の方法を用いて、多くの病原体関連抗原検出系を創出できると期待される。
付記
本研究は、東京工業大学 科学技術創成研究院のWRHI脱コロナ禍プロジェクトの補助を受けて行われた。
用語説明
[用語1] Q-body(Quench body、クエンチ抗体) : 抗体の断片を、部位特異的に蛍光色素で化学修飾した抗体。蛍光色素が抗体内のアミノ酸により消光(Quench)される現象を利用して、蛍光強度の変化によって抗原を検出できる。
[用語2] バイオセンサー : 生体分子が持っている機能を、化学物質の存在や濃度を測定するために活用する化学センサー。
[用語3] 抗体断片 : 通常抗体の、抗原結合部位を含む断片のこと。蛍光修飾のためのリンカーなどを加えたものを、遺伝子組換え法により大腸菌で発現させて比較的容易に構築することができる。
[用語4] 化学修飾 : 生体高分子に含まれる、化合物の特性を決める特定原子団の性質を化学的に変化させ、反応などの機能を変化させること。
[用語5] 抗原抗体反応 : 抗原と、その特定の抗原に対応する抗体が結合して起こるさまざまな現象。免疫反応やアレルギー反応、アナフィラキシー反応などがあたる。
[用語6] 光誘起電子移動 : 光吸収によって励起状態となった蛍光団と、その近傍に存在する原子団(この場合Trp)との間に生じる電子移動。励起された電子は元の軌道に戻れず、蛍光団由来の蛍光がみられなくなる。
[用語7] 色素間相互作用 : ローダミン類などで複数の色素が近接すると、H-dimerと呼ばれる2量体構造を形成し、その蛍光がクエンチする現象。
[用語8] HAタンパク質 : インフルエンザウイルスの主要構成タンパク質であり、感染に必要なヘムアグルチニン酵素。ウイルスの分類にも用いられる。
[用語9] ファージライブラリ : 多くの種類のヒト型抗体の遺伝子を内部に持ち,それがコードするタンパク質を外皮タンパク質に付加する形で発現するファージの集団。固定化抗原に結合するファージを選択することで,特異的抗体の遺伝子を得ることができる。今回は、2018年にタンパク質の分子進化技術開発でノーベル賞を受賞したGregory Winter博士グループ由来のものを使用した。
論文情報 1
掲載誌 : |
Scientific Reports 12, 15496 (2022) |
論文タイトル : |
Isolation of a Human SARS-CoV-2 Neutralizing Antibody from a Synthetic Phage Library and its Conversion to Fluorescent Biosensors |
著者 : |
Haimei Li#, Bo Zhu#, Baowei Li, Limei Chen, Xuerao Ning, Hang Dong, Jingru Liang, Xueying Yang, Jinhua Dong* and Hiroshi Ueda* (#Equal contributions) |
DOI : |
論文情報 2
掲載誌 : |
Analyst 147, 4971-4979 (2022) |
論文タイトル : |
Rapid and sensitive SARS-CoV-2 detection using a homogeneous fluorescent immunosensor Quenchbody with crowding agents |
著者 : |
Bo Zhu#, Nobuyuki Nosaka#, Shuji Kanamaru, Jinhua Dong, Yancen Dai, Akihito Inoue, Yinghui Yang, Kaori Kobayashi, Tetsuya Kitaguchi, Hiroshi Iwasaki, Ryuji Koike, Kenji Wakabayashi and Hiroshi Ueda* (#Equal contributions) |
DOI : |
お問い合わせ先
東京工業大学 科学技術創成研究院 化学生命科学研究所
教授 上田宏
Email ueda@res.titech.ac.jp
Tel / Fax 045-924-5248
取材申し込み先
東京工業大学 総務部 広報課
Email media@jim.titech.ac.jp
Tel 03-5734-2975 / Fax 03-5734-3661
東京医科歯科大学 総務部 総務秘書課 広報係
Email kouhou.adm@tmd.ac.jp
Tel 03-5803-5833 / Fax 03-5803-0272