東工大ニュース
東工大ニュース
公開日:2019.05.13
東京医科大学 ナノ粒子先端医学応用講座の半田宏特任教授(東京工業大学名誉教授)および東京工業大学 生命理工学院の山口雄輝教授らのグループは、サリドマイドが結合する標的タンパク質であるセレブロンが、脳の神経幹細胞の増殖を制御することで、頭部を縮小・拡大させることを、ゼブラフィッシュのモデル系を用いて明らかにしました(図1)。
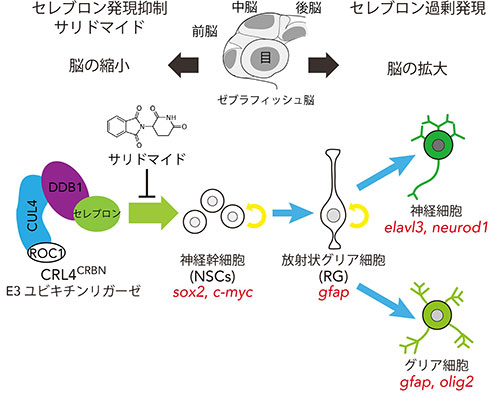
図1. サリドマイド処理とセレブロンの発現抑制・発現増加が脳の発生に及ぼす作用
サリドマイド処理もしくはセレブロンの発現抑制で頭部が縮小し、セレブロンの過剰発現で頭部が拡大する。これらの表現型は、セレブロンが神経幹細胞の増殖を制御していることで説明可能である。
セレブロンは、半世紀前、服用した妊婦の胎児に深刻な奇形を引き起こした薬剤サリドマイドの主要な細胞内標的因子として半田特任教授、東京医科大学 ナノ粒子先端医学応用講座の伊藤 拓水准教授らによって同定され、2010年にScience誌に報告されました。セレブロンは、タンパク質の分解を司るE3ユビキチンリガーゼ複合体の構成因子であり、分解すべき基質タンパク質を認識する役割を担っています。
今回、半田特任教授、山口教授らの国際共同研究グループは、脊椎動物のモデル生物であるゼブラフィッシュを用いて、セレブロンが発生初期の脳において神経幹細胞の増殖を制御し、頭部の縮小や拡大をもたらすことを明らかにしました(図1)。今回の研究成果により、サリドマイドと類似した構造を持つ化合物(サリドマイド類似体)が、セレブロンと結合して、脳の神経幹細胞に増殖に作用する可能性が示唆されました。本研究で得られた知見から、脳の神経幹細胞の増殖を制御する新たな薬剤の開発も期待されます。本研究成果は、米科学誌「iScience」の電子版に4月9日に掲載されました。
サリドマイドは、1950年代に鎮静剤として開発されましたが、妊娠中の女性が服用すると新生児の手足や耳などに発生障害(奇形)をもたらすことから、世界的な薬害を引き起こし、1960年代前半に一度市場から撤退を余儀なくされました。新生児は、サリドマイドに暴露された時期により異なる奇形を示し、妊娠初期に暴露されると自閉症を引き起こします。しかし、サリドマイドが脳の発生にどのように作用するのかは全く明らかにされていませんでした。
研究グループはまず、脊椎動物のモデル生物であるゼブラフィッシュは、サリドマイド処理により頭部が縮小することを示しました(図2)。次に、サリドマイドの標的タンパク質であるセレブロンの発現を抑制すると、頭部原基でp53依存的な細胞死が誘導され、頭部縮小をもたらすことを明らかにしました(図3)。反対に、セレブロンを過剰発現すると頭部が拡大し(図4)、脳の神経幹細胞が増加しました(図5)。セレブロンの過剰発現により、頭部原基が形成される発生初期からSOX2を発現する神経幹細胞が増加し、その結果、神経幹細胞から生み出される神経細胞やグリア細胞も増加していました(図1)。このことが、セレブロン過剰発現による頭部拡大をもたらしていると考えられます。

図2. ゼブラフィッシュ胚の頭部に対するサリドマイドの影響
200 µMもしくは400 µMのサリドマイド存在下で発生したゼブラフィッシュ胚は、より小さな頭部をもつ。
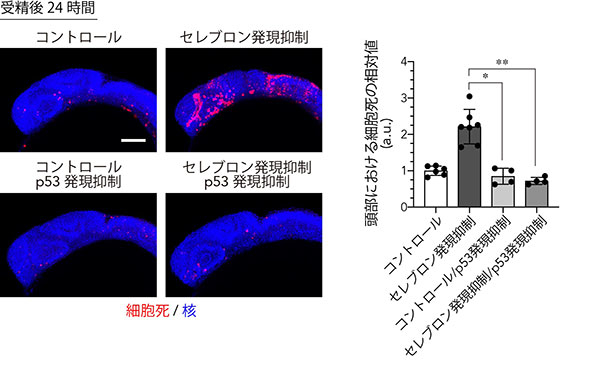
図3. セレブロンの発現抑制は脳でp53依存的に細胞死を誘導する
(左)セレブロンの発現抑制により細胞死(赤い蛍光)が誘導されるが、p53の発現をあらかじめ抑制しておくと細胞死が誘導されない。
(右)細胞死のレベルを定量化したグラフ。
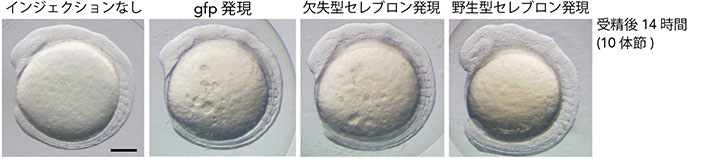
図4. セレブロンの過剰発現による脳の拡大
野生型セレブロンを発現したときのみ、他のコントロールと比較してゼブラフィッシュ胚の頭部が拡大する。
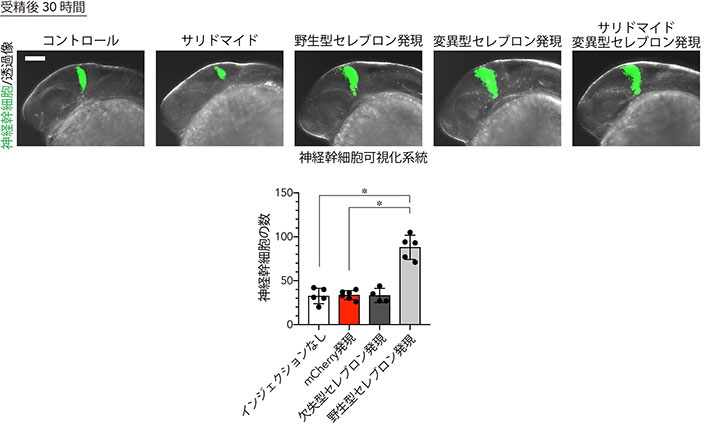
図5. サリドマイド処理とセレブロンの過剰発現が脳の神経幹細胞に及ぼす作用
本研究は、サリドマイドの標的タンパク質であるセレブロンの脳の発生過程における役割を、ゼブラフィッシュのモデル系を用いて初めて明らかにしました。特に、セレブロンの発現が増加すると、脳の神経幹細胞が増えることが分かりました。今回の発見は、セレブロンの活性を高めるサリドマイド類似体を同定すれば、脳の神経幹細胞を増やす作用を持つ新たな薬になる可能性を示唆します。サリドマイドはかつて胎児に深刻な奇形をもたらした薬として世界的に知られていますが、セレブロンの活性を高めるサリドマイド類似体は、今後拡大が予想される認知症や精神疾患等の治療薬となる可能性を秘めています。
論文情報
掲載誌 : |
iScience |
論文タイトル : |
Cereblon Control of Zebrafish Brain Size by Regulation of Neural Stem Cell Proliferation |
著者 : |
Hideki Ando, Tomomi Sato, Takumi Ito, Junichi Yamamoto, Satoshi Sakamoto, Nobuhiro Nitta, Tomoko Asatsuma-Okumura, Nobuyuki Shimizu, Ryota Mizushima, Ichio Aoki, Takeshi Imai, Yuki Yamaguchi, Arnold J.Berk, and Hiroshi Handa |
DOI : |
日本学術振興会 科学研究費補助金 基盤研究(S)「脳神経幹細胞の増殖分化を制御するサリドマイド標的因子セレブロンの新規作動薬の探索」17H06112(半田宏、山口雄輝)
東京医科大学に発足した産学連携講座であり、米国Celgene社がスポンサーを務めています。
お問い合わせ先
東京医科大学 ナノ粒子先端医学応用講座
特任教授 半田宏
E-mail : hhanda@tokyo-med.ac.jp
Tel : 03-5323-3250
東京工業大学 生命理工学院
教授 山口雄輝
E-mail : yyamaguc@bio.titech.ac.jp
Tel : 045-924-5798
取材申し込み先
東京医科大学 総務部広報・社会連携推進課
Tel : 03-3351-6141(代表)
東京工業大学 広報・社会連携本部 広報・地域連携部門
E-mail : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661